题目内容
15.实验室常采用亚硫酸钠(Na2SO3)固体与浓硫酸在常温下反应制取二氧化硫,二氧化硫是一种有毒气体,密度大于空气,易溶于水.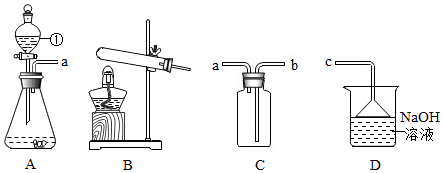
(1)①的仪器名称是分液漏斗.
(2)实验室制取二氧化硫选择的发生装置是A(填字母序号).实验室用该装置还可以制取氧气,写出反应的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.实验室用该装置也可以制取二氧化碳,写出反应的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑.
(3)用如图C所示装置收集二氧化硫时,a(填“a”或“b”)端管口与c管相连,烧杯中氢氧化钠溶液可以吸收多余的二氧化硫,生成亚硫酸钠(Na2SO3)和水,写出该反应的化学方程式SO2+2NaOH=Na2SO3+H2O.
分析 (1)熟记仪器的名称;
(2)根据反应物的状态与反应条件来确定制取装置,根据装置确定制取氧气与二氧化碳的方法;
(3)用上图所示装置C收集二氧化硫时,二氧化硫应该长进短出,因为二氧化硫的密度比空气的密度大,因此a端管口与c管相连;二氧化硫和氢氧化钠反应生成亚硫酸钠和水,配平即可.
解答 解:(1)①仪器的名称分液漏斗;故填:分液漏斗;
(2)实验室常用亚硫酸钠(Na2SO3)固体与浓硫酸在常温下反应制取二氧化硫,因此不需要加热;过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳;故答案为:A;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;CaCO3+2HCl═CaCl2+H2O+CO2↑;
(3)用上图所示装置C收集二氧化硫时,二氧化硫应该长进短出,因为二氧化硫的密度比空气的密度大,因此a端管口与c管相连;二氧化硫和氢氧化钠反应生成亚硫酸钠和水,配平即可;故答案为:a;SO2+2NaOH=Na2SO3+H2O.
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
5.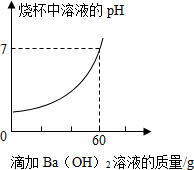 某品牌洁厕灵的成分是硫酸与盐酸的混合溶液,某课外活动小组想测定该品牌洁厕灵溶液中HCl的质量.取20g该品牌的洁厕灵溶液于烧杯中,不断滴加溶质质量分数为17.1%的氢氧化钡溶液,反应过程中烧杯中产生沉淀质量和烧杯中溶液pH变化的部分数据如表所示:(已知BaCl2溶液的pH=7)
某品牌洁厕灵的成分是硫酸与盐酸的混合溶液,某课外活动小组想测定该品牌洁厕灵溶液中HCl的质量.取20g该品牌的洁厕灵溶液于烧杯中,不断滴加溶质质量分数为17.1%的氢氧化钡溶液,反应过程中烧杯中产生沉淀质量和烧杯中溶液pH变化的部分数据如表所示:(已知BaCl2溶液的pH=7)
求:
(1)完全反应后生成沉淀的质量为4.66g;
(2)计算该洁厕灵溶液中HCl的质量分数为多少?(计算结果保留至0.1%)
 某品牌洁厕灵的成分是硫酸与盐酸的混合溶液,某课外活动小组想测定该品牌洁厕灵溶液中HCl的质量.取20g该品牌的洁厕灵溶液于烧杯中,不断滴加溶质质量分数为17.1%的氢氧化钡溶液,反应过程中烧杯中产生沉淀质量和烧杯中溶液pH变化的部分数据如表所示:(已知BaCl2溶液的pH=7)
某品牌洁厕灵的成分是硫酸与盐酸的混合溶液,某课外活动小组想测定该品牌洁厕灵溶液中HCl的质量.取20g该品牌的洁厕灵溶液于烧杯中,不断滴加溶质质量分数为17.1%的氢氧化钡溶液,反应过程中烧杯中产生沉淀质量和烧杯中溶液pH变化的部分数据如表所示:(已知BaCl2溶液的pH=7)| 滴加氢氧化钡溶液的质量/g | 5 | 10 | 25 |
| 烧杯中产生沉淀的质量/g | 1.165 | 2.33 | 4.66 |
(1)完全反应后生成沉淀的质量为4.66g;
(2)计算该洁厕灵溶液中HCl的质量分数为多少?(计算结果保留至0.1%)
6.如图为某矿泉水标签的部分内容,下列说法正确的是( )


| A. | 该矿泉水是蒸馏水 | B. | 该矿泉水中可能含有CaCl2 | ||
| C. | 偏硅酸中硅元素的化合价为+6 | D. | 其中K+、Cl均为金属阳离子 |
10.下列各组物质充分混合物后,所得溶液的质量比反应前溶液的总质量减小的是( )
| A. | 盐酸和铜 | B. | 铝和稀硫酸 | ||
| C. | 氯化钠和水 | D. | 铁皮和硫酸铜溶液 |