题目内容
完成以下填空内容
(1)将医用脱脂棉隔绝空气加热时,能生成碳和水,根据这一事实推断:脱脂棉是由 元素组成的.
(2)将100g 10%的过氧化氢溶液和少量二氧化锰混合,完全反应后,所得溶液中H、O两种元素的质量比 .
(3)有一在空气中暴露过的NaOH固体,经分析知其含水7.65%,含Na2CO3 4.32%,其余是NaOH.若将此样品1g放入100g3.65%的稀盐酸中充分反应,残余的酸再用10g 30.9%的NaOH溶液恰好完全中和.将反应后的溶液蒸干,得到固体的质量是 g.
(1)将医用脱脂棉隔绝空气加热时,能生成碳和水,根据这一事实推断:脱脂棉是由
(2)将100g 10%的过氧化氢溶液和少量二氧化锰混合,完全反应后,所得溶液中H、O两种元素的质量比
(3)有一在空气中暴露过的NaOH固体,经分析知其含水7.65%,含Na2CO3 4.32%,其余是NaOH.若将此样品1g放入100g3.65%的稀盐酸中充分反应,残余的酸再用10g 30.9%的NaOH溶液恰好完全中和.将反应后的溶液蒸干,得到固体的质量是
考点:质量守恒定律及其应用,元素质量比的计算,根据化学反应方程式的计算
专题:化学式的计算,化学用语和质量守恒定律
分析:(1)化学反应前后,元素的种类不变,原子的种类、总个数不变;
(2)过氧化氢在二氧化锰的催化作用下分解生成水和氧气;
(3)碳酸钠和稀盐酸反应生成氯化钠、水额二氧化碳,氢氧化钠和稀盐酸反应生成氯化钠和水,将反应后的溶液蒸干,得到固体是氯化钠,根据100g3.65%的稀盐酸可以计算生成氯化钠的质量.
(2)过氧化氢在二氧化锰的催化作用下分解生成水和氧气;
(3)碳酸钠和稀盐酸反应生成氯化钠、水额二氧化碳,氢氧化钠和稀盐酸反应生成氯化钠和水,将反应后的溶液蒸干,得到固体是氯化钠,根据100g3.65%的稀盐酸可以计算生成氯化钠的质量.
解答:解:(1)将医用脱脂棉隔绝空气加热时,能生成碳和水,根据质量守恒定律可知,脱脂棉是由碳元素、氢元素和氧元素组成的.
故填:碳、氢 和氧.
(2)完全反应后,得到的液体是H2O,水中H、O两种元素的质量比为:(1×2):(16×1)=1:8,
故填:1:8.
(3)设生成氯化钠的质量为x,
由Na2CO3+2HCl═2NaCl+H2O+CO2↑,NaOH+HCl═NaCl+H2O可知,HCl→NaCl,
HCl→NaCl,
36.5 58.5
100g×3.65% x
=
,
x=5.85g,
故填:5.85.
故填:碳、氢 和氧.
(2)完全反应后,得到的液体是H2O,水中H、O两种元素的质量比为:(1×2):(16×1)=1:8,
故填:1:8.
(3)设生成氯化钠的质量为x,
由Na2CO3+2HCl═2NaCl+H2O+CO2↑,NaOH+HCl═NaCl+H2O可知,HCl→NaCl,
HCl→NaCl,
36.5 58.5
100g×3.65% x
| 36.5 |
| 100g×3.65% |
| 58.5 |
| x |
x=5.85g,
故填:5.85.
点评:化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
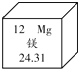 镁有“国防金属”的美誉.在元素周期表中,镁元素的信息如图所示,对图中信息解释不正确的是( )
镁有“国防金属”的美誉.在元素周期表中,镁元素的信息如图所示,对图中信息解释不正确的是( )| A、原子序数为12 |
| B、元素符号为Mg |
| C、原子核外电子数为24 |
| D、相对原子质量为24.31 |
下列化学方程式书写正确的是( )
A、4Fe+3O2
| ||||
B、2H2+O2
| ||||
| C、CaO+H2O=Ca(OH)2 | ||||
| D、CuSO4+H2O=CuSO4?5H2O |
在一只密闭容器内有四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表,下列说法正确的是( )
| 物质 | X | Y | Z | Q |
| 反应前质量/g | 8 | 2 | 40 | 5 |
| 反应后质量/g | 待测 | 24 | 8 | 23 |
| A、反应后X的质量为0 |
| B、Y、Q的相对分子质量比一定为11:9 |
| C、参加反应的X、Z的质量比为1:5 |
| D、该密闭容器中发生的化学变化属于分解反应 |
下列物质的用途中,主要应用其化学性质的是( ),请在D处补充符合题意的一个答案.
| A、用石墨制铅笔芯 |
| B、用铁、铝制作炊具 |
| C、用盐酸除铁锈 |
| D、用一氧化碳炼铁 |
“物质的量”是国际单位制中的一个基本物理量,有关说法正确的是( )
| A、质量相等的O2和O3,他们的物质的量之比为2:3 |
| B、1mol氧气的摩尔质量为32 |
| C、1mol任何物质都含有6.02×1023个原子 |
| D、2克H2中含有1mol氢分子 |
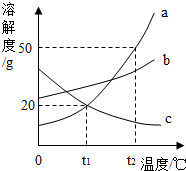 如图是a、b、c三种固体物质的溶解度曲线.
如图是a、b、c三种固体物质的溶解度曲线.