题目内容
12.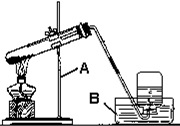 高锰酸钾制取并收集氧气的装置如下:
高锰酸钾制取并收集氧气的装置如下:(1)写出 A,B仪器的名称
A铁架台;B水槽
(2)这个图有三处明显的错误,请指出错误
并改正:
①试管口未塞棉花②试管口未略向下倾斜③伸入试管的导管过长
(3)实验完毕后,应该先移导气管,后熄灭酒精灯,其原因是
若先熄灭酒精灯,试管温度降低,压强变小,水槽中的水会倒流炸裂试管
(4)图中收集氧气的方法叫排水法,这是因为氧气不易溶于水.收集满氧气的集气瓶要盖好玻璃片,并正(填“正”或“倒”)放在桌上.
(5)实验结束时,发现收集到的氧气不纯,可能的原因是:①未等气泡连续、均匀冒出就开始收集;②集气瓶内未装满水.
(6)写出试管中发生反应的文字表达式.高锰酸钾 $\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气.
分析 据题意知,要了解正确的实验装置,才能找出错误,并首先要注意找明显的地方,实验过程中的注意事项要做到心中有数;并认识实常见的试验仪器.
解答 解:
(1)根据图中所标,知A 是铁架台,B 是水槽;
(2)根据与正确装置的对比和原理可知,试管口未塞棉花,试管的夹持位置不对,试管口不该向上,伸到试管的导管过长而不利于氧气的排出和装置中原有空气排不干净,集气瓶中的导管过短,无法排除瓶中的空气.
(3)实验完毕后,应该先移导气管,后熄灭酒精灯,其原因是:若先熄灭酒精灯,试管温度降低,压强变小,水槽中的水会倒流炸裂试管;
故答案为:若先熄灭酒精灯,试管温度降低,压强变小,水槽中的水会倒流炸裂试管;
(4)图中收集氧气的方法是排水法,因为氧气不易溶于水;氧气的密度比空气大,所以收满氧气的集气瓶要盖好玻璃片,正放在桌子上;
故答案为:排水法;不易溶于水;正;
(5)实验结束时,发现收集到的氧气不纯,可能的原因是:未等气泡连续、均匀冒出就开始收集,此时的氧气中混有空气;可能集气瓶内未装满水,混入部分空气;
故答案为:①未等气泡连续、均匀冒出就开始收集;②集气瓶内未装满水;
(6)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气;由一种物质反应生成三种物质,符合分解反应的特点,属于分解反应;
故答案为:
(1)铁架台;水槽;
(2)试管口未塞棉花;试管口未略向下倾斜;伸入试管的导管过长;
(3)若先熄灭酒精灯,试管温度降低,压强变小,水槽中的水会倒流炸裂试管;
(4)排水法;不易溶于水;正;
(5)①未等气泡连续、均匀冒出就开始收集;②集气瓶内未装满水;
(6)高锰酸钾 $\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;
点评 应熟悉初中化学中常见的仪器,明确仪器的使用及注意问题,在具体的实验中要注意规范和原理来确保实验的成功.

| A. | S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 | B. | H2O2$\frac{\underline{\;MnO_2\;}}{\;}$H2O+O2↑ | ||
| C. | 6HCl+2Fe═2FeCl3+3H2↑ | D. | Fe2O3+3CO═2Fe+3CO2 |
| A. | 12:1 | B. | 6:1 | C. | 4:1 | D. | 1:1 |

(1)实验中可观察到玻璃管中铜丝的颜色由红色变成黑色;
(2)铜丝在氧气中反应的文字表达式是铜+氧气$\stackrel{加热}{→}$氧化铜;
(3)如表是三个实验小组的实验数据:
| 组别 | 甲 | 乙 | 丙 |
| 实验前注射器中气体的体积 | 30毫升 | 30毫升 | 30毫升 |
| 实验后注射器中气体的体积 | 29毫升 | 27毫升 | 28毫升 |
| 前后气体的体积差 | 1毫升 | 3毫升 | 2毫升 |
②从上述实验结果分析,误差都较大,试分析可能由哪几种原因引起的(写出两条)铜丝的量不足;装置的漏气.
(4)丙组的同学在实验过程中,认为加热铜丝反应较慢,想把铜丝改为木炭,你不为是否可以不可以(填可以或不可以),为什么?木炭可以和氧气反应生成二氧化碳气体,不能产生压强差.
(5)在实验室中用过氧化氢溶液和二氧化锰制取氧气,选择的发生装置是(如图2中)B(填序号),写出反应的文字表达式过氧化氢$\stackrel{二氧化锰}{→}$氧气+水;
(6)用C装置收集氧气时,应将该装置的a端与发生装置连接.
| A. | 铁在空气中容易生锈,铝在空气中更容易锈蚀 | |
| B. | 中和反应一定生成盐和水,生成盐和水的反应一定是中和反应 | |
| C. | 有机物都含有碳元素,含有碳元素的物质不一定是有机物 | |
| D. | 电解水生成氢气和氧气,所以水是由氢气和氧气组成 |