题目内容
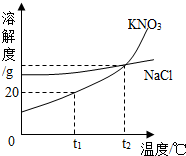 如图是KNO3和NaCl的溶解度曲线.下列说法中正确的是( )
如图是KNO3和NaCl的溶解度曲线.下列说法中正确的是( )| A、将NaCl和KNO3的饱和溶液分别由t2℃降温到t1℃,析出的KNO3多 |
| B、t2℃时,NaCl和KNO3的溶液中溶质的质量分数相等 |
| C、t1℃时,100 g KNO3的饱和溶液中含有20 g KNO3 |
| D、最好用蒸发溶剂的方法分离出混有少量KNO3的NaCl固体 |
考点:固体溶解度曲线及其作用,结晶的原理、方法及其应用,晶体和结晶的概念与现象,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:A、由KNO3和NaCl的溶解度曲线可知,氯化钠的溶解度受温度的影响变化不大,硝酸钾的溶解度随温度的升高而增大,KNO3、NaCl饱和溶液的温度从t2℃降到t1℃时,KNO3先析出晶体;
B、由于在t2℃时,两物质的溶解度相等,NaCl的饱和溶液与KNO3的饱和溶液中溶质的质量分数相等;
C、根据t1℃时,硝酸钾的溶解度解答;
D、根据物质的溶解度会随温度的变化而变化来确定;
B、由于在t2℃时,两物质的溶解度相等,NaCl的饱和溶液与KNO3的饱和溶液中溶质的质量分数相等;
C、根据t1℃时,硝酸钾的溶解度解答;
D、根据物质的溶解度会随温度的变化而变化来确定;
解答:解:
A、由KNO3和NaCl的溶解度曲线可知,氯化钠的溶解度受温度的影响变化不大,硝酸钾的溶解度随温度的升高而增大,KNO3、NaCl饱和溶液的温度从t2℃降到t1℃时,KNO3先析出晶体,由于饱和溶液质量无法比较,不能确定析出晶体的多少,故错;
B、由于在t2℃时,两物质的溶解度相等,NaCl的饱和溶液与KNO3的饱和溶液中溶质的质量分数相等,故错;
C、t1℃时,硝酸钾的溶解度是20g,说明100g水中溶解20g硝酸钾,KNO3饱和溶液质量为120g,故错.
D、由KNO3和NaCl的溶解度曲线可知,氯化钠的溶解度受温度的影响变化不大,硝酸钾的溶解度随温度的升高而增大,任何物质的溶液都可通过的方法使溶质结晶析出.若分别从KNO3、NaCl的纯溶液中提取KNO3、NaCl晶体,应采用蒸发溶剂的方法,若从含少量KNO3的NaCl固体,宜采用蒸发溶剂;故对.
答案:D
A、由KNO3和NaCl的溶解度曲线可知,氯化钠的溶解度受温度的影响变化不大,硝酸钾的溶解度随温度的升高而增大,KNO3、NaCl饱和溶液的温度从t2℃降到t1℃时,KNO3先析出晶体,由于饱和溶液质量无法比较,不能确定析出晶体的多少,故错;
B、由于在t2℃时,两物质的溶解度相等,NaCl的饱和溶液与KNO3的饱和溶液中溶质的质量分数相等,故错;
C、t1℃时,硝酸钾的溶解度是20g,说明100g水中溶解20g硝酸钾,KNO3饱和溶液质量为120g,故错.
D、由KNO3和NaCl的溶解度曲线可知,氯化钠的溶解度受温度的影响变化不大,硝酸钾的溶解度随温度的升高而增大,任何物质的溶液都可通过的方法使溶质结晶析出.若分别从KNO3、NaCl的纯溶液中提取KNO3、NaCl晶体,应采用蒸发溶剂的方法,若从含少量KNO3的NaCl固体,宜采用蒸发溶剂;故对.
答案:D
点评:本题难度不大,主要考查了固体溶解度曲线所表示的意义,通过本题可以加强学生对固体溶解度的理解,培养学生应用知识解决问题的能力.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
下列有关质量守恒定律的认识,不正确的是( )
| A、质量守恒定律为揭示化学变化的规律,提供了理论依据 |
| B、通过化学变化,只能改变世界上物质的种类,不能改变物质的总质量 |
| C、质量守恒定律揭示了化学变化中宏观物质之间的质量关系,与微观过程无关 |
| D、所有的化学变化都遵守质量守恒定律 |
区分硫粉、高锰酸钾、二氧化锰三种固体,最好的方法是( )
| A、加热法 | B、溶解法 |
| C、观察法 | D、称量法 |
化学变化的本质特征是( )
| A、有颜色变化 |
| B、有气体放出 |
| C、放出热量 |
| D、有新物质生成 |
下列灭火措施不合理的是( )
| A、森林火灾,可开辟隔离带,防止火势蔓延 |
| B、油锅起火,应立即盖上锅盖并关闭火源 |
| C、不小心碰倒酒精灯在桌上燃烧起来,应立即用湿抹布盖灭 |
| D、电线或家用电器着火时,应立即用水扑灭 |
不用其它任何试剂,下列物质①MgSO4 ②NaOH ③CuCl2 ④KCl ⑤Ba(NO3)2被鉴别出来的顺序正确的是( )
| A、①②③④⑤ |
| B、③②①⑤④ |
| C、③②④⑤① |
| D、④③①②⑤ |
下列物质不能导电的是( )
| A、蔗糖溶液 | B、食盐溶液 |
| C、稀硫酸 | D、金属铜 |
 课外活动中,化学兴趣小组的同学们用A、B、C、D、E(分别为H2O、CO2、H2、Fe、Fe3O4中的一种)进行“化学反应接龙”游戏,游戏规则是:前一种物质分解或与其他物质反应而生成下一种物质,请按要求回答下列问题:若B在空气中燃烧产生淡蓝色火焰,则:
课外活动中,化学兴趣小组的同学们用A、B、C、D、E(分别为H2O、CO2、H2、Fe、Fe3O4中的一种)进行“化学反应接龙”游戏,游戏规则是:前一种物质分解或与其他物质反应而生成下一种物质,请按要求回答下列问题:若B在空气中燃烧产生淡蓝色火焰,则: