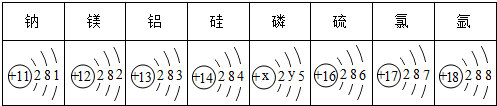
题目内容
含碳酸钙80%的石灰石12.5g,与94.4g某稀盐酸恰好完全反应.反应的化学方程式为:CaCO3+2HCl═CaCl2+CO2↑+H2O.请计算:
(1)生成的二氧化碳的质量;
(2)反应后所得溶液中溶质的质量分数.
(1)生成的二氧化碳的质量;
(2)反应后所得溶液中溶质的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:(1)根据化学方程式利用碳酸钙的质量计算二氧化碳的质量;
(2)根据化学方程式利用碳酸钙的质量计算出氯化钙的质量,再根据反应后所得溶液的质量求质量分数.
(2)根据化学方程式利用碳酸钙的质量计算出氯化钙的质量,再根据反应后所得溶液的质量求质量分数.
解答:解:设生成二氧化碳的质量为X,同时生成氯化钙的质量为Y
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 111 44
12.5g×80% y x
=
=
解得:x=4.4g y=11.1g
(1)生成的二氧化碳的质量为4.4g;
(2)反应后所得氯化钙溶液中溶质的质量分数为:
×100%=11.1%;
答:生成二氧化碳的质量为4.4克,同时生成氯化钙溶液的质量分数为11.1%.
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 111 44
12.5g×80% y x
| 100 |
| 44 |
| 12.5g×80% |
| x |
| 100 |
| 111 |
| 12.5g×80% |
| y |
解得:x=4.4g y=11.1g
(1)生成的二氧化碳的质量为4.4g;
(2)反应后所得氯化钙溶液中溶质的质量分数为:
| 11.1g |
| 12.5g×80%+94.4g-4.4g |
答:生成二氧化碳的质量为4.4克,同时生成氯化钙溶液的质量分数为11.1%.
点评:反应后所得溶液的质量等于碳酸钙的质量与盐酸的质量之和减去生成的二氧化碳的质量.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量百分含量如图所示,下列说法正确的是( )
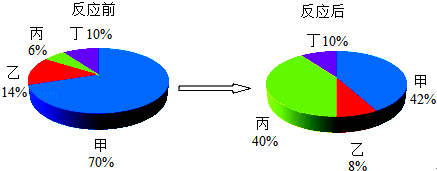

| A、该反应是置换反应 |
| B、该反应是化合反应 |
| C、该反应是分解反应 |
| D、该反应中丁可能是催化剂 |
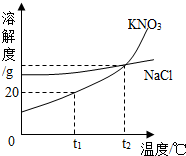 如图是KNO3和NaCl的溶解度曲线.下列说法中正确的是( )
如图是KNO3和NaCl的溶解度曲线.下列说法中正确的是( )| A、将NaCl和KNO3的饱和溶液分别由t2℃降温到t1℃,析出的KNO3多 |
| B、t2℃时,NaCl和KNO3的溶液中溶质的质量分数相等 |
| C、t1℃时,100 g KNO3的饱和溶液中含有20 g KNO3 |
| D、最好用蒸发溶剂的方法分离出混有少量KNO3的NaCl固体 |
如图,下列实验操作正确的是( )
A、 |
B、 |
C、 |
D、 |