题目内容
12.现在正值冬季,天气寒冷.人们都喜欢吃火锅,常用的火锅燃料是一种俗称“固体酒精”的物质.已知“固体酒精”是用酒精、醋酸钙和水按一定比例制成的“胶东”.若点燃“固体酒精”时只有酒精发生燃烧,现取30g“固体酒精”完全燃烧后生成44g二氧化碳.请计算“固体酒精”中酒精的质量分数是多少?(结果保留0.1%)分析 酒精燃烧生成二氧化碳和水,由生成二氧化碳的质量根据反应的化学方程式计算出参加反应的酒精的质量即可计算酒精的质量分数.
解答 解:设酒精的质量为x
C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O
46 88
x 44g
$\frac{46}{88}=\frac{x}{44g}$
x=23g
故酒精的质量分数为:$\frac{23g}{30g}×100%$≈76.7%
答:“固体酒精”中酒精的质量分数是76.7%.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目
2.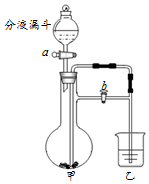 化学小组同学利用如图装置分别完成2个实验.
化学小组同学利用如图装置分别完成2个实验.
(1)实验1:打开b和a,将分液漏斗中过量的盐酸注入,关闭a,此时乙中反应的化学方程式是Ca(OH)2+CO2=CaCO3↓+H2O,一段时间后,关闭b,观察到乙中液体变澄清,产生此现象的原因是甲中压强增大,使稀盐酸进入到乙中,与难溶于水的碳酸钙发生反应.
(2)实验2:观察到乙中白磷的现象是融化,但不燃烧;打开b和a,当分液漏斗中的过氧化氢溶液全部注入后,关闭a,观察到乙中白磷的现象是白磷燃烧.关闭b,一段时间后,白磷的现象及原因是虽然因甲中压强增大,进入到乙中的过氧化氢受热分解生成了氧气,但氧气量少,不足以使白磷燃烧.
 化学小组同学利用如图装置分别完成2个实验.
化学小组同学利用如图装置分别完成2个实验.| 序号 | 甲 | 乙 | 分液漏斗 |
| 1 | 大理石 | 澄清石灰水 | 稀盐酸 |
| 2 | 二氧化锰 | 80℃热水及一小块白磷 | 过氧化氢溶液 |
(2)实验2:观察到乙中白磷的现象是融化,但不燃烧;打开b和a,当分液漏斗中的过氧化氢溶液全部注入后,关闭a,观察到乙中白磷的现象是白磷燃烧.关闭b,一段时间后,白磷的现象及原因是虽然因甲中压强增大,进入到乙中的过氧化氢受热分解生成了氧气,但氧气量少,不足以使白磷燃烧.
17.一杯氯化钠溶液的质量分数为15%,关于此溶液说法正确的是( )
| A. | 100克水中含氯化钠15克 | |
| B. | 100克氯化钠溶液中含氯化钠15克 | |
| C. | 100克水中最多可溶解15克氯化钠 | |
| D. | 将溶液倒出一半后,质量分数变为7.5% |
4.一定温度下将a%硝酸钾溶液分成两等份,一份等温蒸发10克水,得到m克无水晶体:另一份等温蒸发20克水,得到3m克无水晶体,则该温度下硝酸钾的溶解度为( )
| A. | 10m克 | B. | 20m克 | C. | 30m克 | D. | $\frac{1000a}{100-a}$克 |
 材料对我们的生活影响越来越大
材料对我们的生活影响越来越大