题目内容
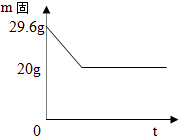 某实验小组,混合27.6g氯酸钾和2g二氧化锰,加热支取一定量氧气后撤去酒精灯,测得剩余固体质量如图所示.计算:
某实验小组,混合27.6g氯酸钾和2g二氧化锰,加热支取一定量氧气后撤去酒精灯,测得剩余固体质量如图所示.计算:(1)制得氧气的质量为
(2)氯酸钾分解的质量分数
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:(1)依据混合物加热后固体质量减小的值即为氧气的质量分析解答;
(2)依据氧气的质量求出分解的氯酸钾的质量,进而求出氯酸钾分解的质量分数;
(2)依据氧气的质量求出分解的氯酸钾的质量,进而求出氯酸钾分解的质量分数;
解答:解:(1)由质量守恒定律可知生成氧气的质量是29.6g-20g=9.6g;
(2)解:设分解的氯酸钾的质量为x
2KClO3
2KCl+3O2↑
245 96
x 9.6g
=
x=24.5g
分解的氯酸钾的质量分数为:
×100%=88.8%
答:氯酸钾分解的质量分数为88.8%.
故答案为:(1)9.6;(2)为88.8%.
(2)解:设分解的氯酸钾的质量为x
2KClO3
| ||
| △ |
245 96
x 9.6g
| 245 |
| x |
| 96 |
| 9.6g |
x=24.5g
分解的氯酸钾的质量分数为:
| 24.5g |
| 27.6g |
答:氯酸钾分解的质量分数为88.8%.
故答案为:(1)9.6;(2)为88.8%.
点评:本题主要考查质量守恒定律,固体反应前后减少的质量为生成氧气的质量是解决此题的关键.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
化学反应遵守质量守恒的原因,是在反应中( )
| A、物质的种类没有改变 |
| B、分子的种类没有改变 |
| C、原子的种类、数目和质量都没有改变 |
| D、分子的数目没有改变 |
下列实验设计方案合理的是( )
| A、用碳酸钾和氢氧化镁制备氢氧化钾 |
| B、用氯化钙溶液检验氢氧化钠是否部分变质 |
| C、用氢氧化钡溶液区分硫酸镁和硫酸钠 |
| D、用氢氧化钠溶液和浓硫酸除去二氧化碳中混有的氯化氢和水蒸气 |
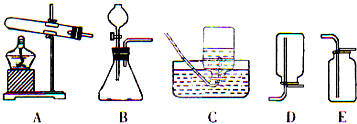

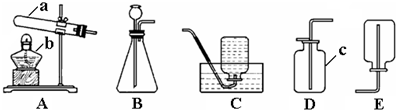
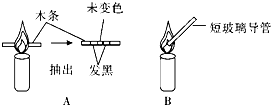 某化学兴趣小组的两位同学对蜡烛燃烧进行了如下探究,请你完成其中的一些步骤.
某化学兴趣小组的两位同学对蜡烛燃烧进行了如下探究,请你完成其中的一些步骤.