题目内容
3. 为探究物质的燃烧条件,某同学进行了如右图所示的实验,下列有关说法正确的是( )
为探究物质的燃烧条件,某同学进行了如右图所示的实验,下列有关说法正确的是( )| A. | 现象③说明红磷不是可燃物 | |
| B. | 现象②③说明物质燃烧需要氧气 | |
| C. | 现象①③说明白磷的着火点比红磷的着火点低 | |
| D. | 现象①②说明物质的燃烧需要达到一定的温度 |
分析 A.红磷是可燃物;
B.现象②是因为没有达到着火点,现象③是因为不与氧气接触;
C.现象①③不同是因为与氧气(或空气)的接触不同;
D.现象②是因为没有达到着火点,现象①是因为满足燃烧的条件.
解答 解:A.水中上的白磷不燃烧,是因为没有与氧气接触,不能说明红磷不是可燃物,故错误;
B.现象②是因为没有达到着火点,现象③是因为不与氧气接触,因此不能说明物质燃烧需要氧气,故错误;
C.现象①③不同是因为铜片上的白磷满足了物质燃烧的三个条件,水中的白磷不能燃烧是因为不与氧气接触,故错误;
D.现象①是因为满足了燃烧的三个条件,现象②是因为没有达到着火点,说明燃烧需要温度,故正确.
故选D.
点评 本题主要检测学生对“燃烧需要同时满足三个条件”这一知识点的掌握情况.

练习册系列答案
相关题目
14.下列特产制作的主要过程中涉及化学变化的是( )
| A. | 奉节脐橙榨汁 | B. | 缙云竹笋晾干 | C. | 梁平金柚酿酒 | D. | 湛江海椒磨粉 |
18.根据如图水分子分解的微观示意图,得出的信息错误的是( )


| A. | 反应前后分子的数目发生改变 | |
| B. | 反应前后分子的种类发生改变 | |
| C. | 分子是化学变化中的最小微粒 | |
| D. | 甲、乙、丙三种分子的个数比为2:2:1 |
15.实验探究是化学的灵魂,请你参与实验室制取氧气和二氧化碳的探究活动.
Ⅰ.制取氧气方法的分析
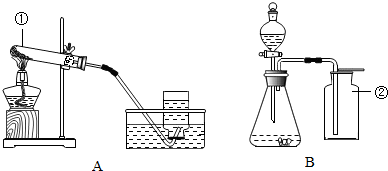
(1)写出A、B装置中标号仪器名称:①试管;②集气瓶.
(2)写出一个用A或B装置制取氧气的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑或2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)若用B装置制取一瓶氧气,验满的方法是将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了.
(4)上述两种方法中,更符合“低碳”理念的是B(填“A”或“B”).
Ⅱ.制取二氧化碳原料的选择
(1)实验室常用大理石或石灰石(主要成分CaCO3)与稀盐酸反应制取二氧化碳,反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O.
(2)实验过程中,同学们提出了下列问题并在老师指导下进行实验.
[问题一]能否用稀硫酸与块状石灰石反应制取二氧化碳?
[实验一]
[分析一]实验室不能(填“能”或“不能”)用稀硫酸与块状石灰石反应制取二氧化碳.
[问题二]能否用粉末状的石灰石、碳酸钙粉末或碳酸钠粉末与稀盐酸反应制取二氧化碳?
[实验二]
[分析二]实验室不选用石灰石粉末、碳酸钙粉末或碳酸钠粉末制取二氧化碳的理由是反应速率太快,不利于二氧化碳的收集.
[结论]实验室制取二氧化碳,原料通常用块状石灰石(或大理石)和稀盐酸.
Ⅲ.拓展与反思
通过探究活动,你认为选择实验方法时应考虑的因素有反应速率快慢(写一种即可).
Ⅰ.制取氧气方法的分析

(1)写出A、B装置中标号仪器名称:①试管;②集气瓶.
(2)写出一个用A或B装置制取氧气的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑或2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)若用B装置制取一瓶氧气,验满的方法是将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了.
(4)上述两种方法中,更符合“低碳”理念的是B(填“A”或“B”).
Ⅱ.制取二氧化碳原料的选择
(1)实验室常用大理石或石灰石(主要成分CaCO3)与稀盐酸反应制取二氧化碳,反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O.
(2)实验过程中,同学们提出了下列问题并在老师指导下进行实验.
[问题一]能否用稀硫酸与块状石灰石反应制取二氧化碳?
[实验一]
| 实验步骤 | 实验现象 |
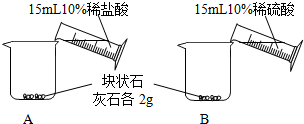 | A中不断产生气泡,固体逐渐减少,有少量固体剩余. B中开始有少量气泡产生,反应很快停止. |
[问题二]能否用粉末状的石灰石、碳酸钙粉末或碳酸钠粉末与稀盐酸反应制取二氧化碳?
[实验二]
| 实验步骤 | 实验现象 |
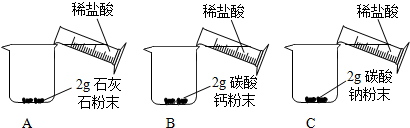 | A中迅速产生大量气泡,固体很快减少,有少量固体剩余. B、C中都迅速产生大量气泡,固体很快消失. |
[结论]实验室制取二氧化碳,原料通常用块状石灰石(或大理石)和稀盐酸.
Ⅲ.拓展与反思
通过探究活动,你认为选择实验方法时应考虑的因素有反应速率快慢(写一种即可).
12.下列物质的用途中,主要利用其化学性质的是( )
| A. | 铜丝做导线 | B. | 干冰用作制冷剂 | ||
| C. | 澄清石灰水检验二氧化碳 | D. | 石墨制铅笔芯 |
13.2011年5月,媒体曝光台湾塑化剂污染食品事件,污染的食品超500多种,是台湾30年来最严重的食品渗毒事件.塑化剂的化学式为C24H38O4,下列说法正确的是( )
| A. | 塑化剂的每一个分子中含有66个原子 | |
| B. | 塑化剂中氢元素的质量分数最高 | |
| C. | 塑化剂是由碳、氢、氧原子构成的 | |
| D. | 塑化剂中碳、氢、氧元素的质量比是24:38:4: |