题目内容
 如图是工业上炼铁的简易图示.某炼铁厂用1000t含氧化铁80%的赤铁矿石炼铁,根据图示回答下列问题:
如图是工业上炼铁的简易图示.某炼铁厂用1000t含氧化铁80%的赤铁矿石炼铁,根据图示回答下列问题:(1)设备A的名称是
(2)理论上可以炼出含杂质4%的生铁的质量是多少?
考点:铁的冶炼,含杂质物质的化学反应的有关计算
专题:金属与金属材料
分析:(1)根据炼铁的设备来分析;(2)由赤铁矿石的质量、氧化铁的质量分数,根据赤铁矿炼铁的化学方程式可以列式计算出炼出生铁的质量即可.
解答:解:(1)炼铁的设备是高炉;故填:高炉;
(2)解:设可炼出含杂质4%的生铁的质量为x.
Fe2O3+3CO
2Fe+3CO2
160 112
1000t×80% (1-4%)x
160:112=(1000t×80%):[(1-4%)x]
x≈583.3t.
答:可炼出含杂质4%的生铁的质量为583.3t.
(2)解:设可炼出含杂质4%的生铁的质量为x.
Fe2O3+3CO
| ||
160 112
1000t×80% (1-4%)x
160:112=(1000t×80%):[(1-4%)x]
x≈583.3t.
答:可炼出含杂质4%的生铁的质量为583.3t.
点评:本题难度不大,考查含杂质物质的化学方程式的计算,注意代入方程式计算的必须是纯物质的质量是正确解答此类题的关键.

练习册系列答案
相关题目

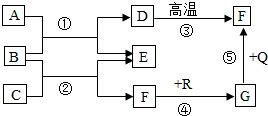 如图是初中化学中常见物质间的转化关系,其中,在通常情况下,F、G是组成元素相同的两种气体,Q、R都是黑色固体(部分反应条件略去),试回答下列问题:
如图是初中化学中常见物质间的转化关系,其中,在通常情况下,F、G是组成元素相同的两种气体,Q、R都是黑色固体(部分反应条件略去),试回答下列问题: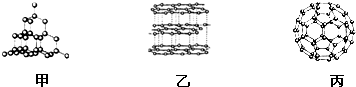
 调味剂的主要作用是补充、增强或增加食品的味道.食醋是一种能增强食品酸味的调味剂,其中约含有3%-5%的醋酸(CH3COOH),醋酸与我们生活密切相联.根据所学知识回答:
调味剂的主要作用是补充、增强或增加食品的味道.食醋是一种能增强食品酸味的调味剂,其中约含有3%-5%的醋酸(CH3COOH),醋酸与我们生活密切相联.根据所学知识回答: