题目内容
7.将干燥的氯酸钾与二氧化锰的混合固体16g放到大试管中加热,完全反应后,冷却到反应前的温度,称量得剩余固体的质量为11.2g.(1)求反应生成氧气的质量为4.8g;
(2)原混合固体中氯酸钾的质量为多少?
分析 氯酸钾在二氧化锰催化作用下受热分解生成氯化钾和氧气,反应前后的质量差即为反应生成氧气的质量,根据氧气质量可以计算氯酸钾质量.
解答 解:(1)反应生成氧气的质量为:16g-11.2g=4.8g,
故填:4.8.
(2)设原混合固体中氯酸钾的质量为x,
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,
245 96
x 4.8g
$\frac{245}{x}$=$\frac{96}{4.8g}$,
x=12.25g,
答:氯酸钾质量是12.25g.
点评 差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解.

练习册系列答案
相关题目
20.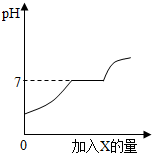 现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH 随滴入X的量的变化关系如图所示.则 X 是( )
现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH 随滴入X的量的变化关系如图所示.则 X 是( )
 现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH 随滴入X的量的变化关系如图所示.则 X 是( )
现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH 随滴入X的量的变化关系如图所示.则 X 是( )| A. | 稀盐酸 | B. | 澄清石灰水 | C. | 水 | D. | 纯碱溶液 |
18.下列物质在氧气中燃烧,能产生白烟的是( )
| A. | 木炭 | B. | 硫 | C. | 磷 | D. | 细铁丝 |
16.以往生产自来水使用适量的氯气,因为氯气可以和水反应得到HCl和HClO(次氯酸),HClO 能杀菌消毒.而新型净水剂高铁酸钠(Na2FeO4)的效果更好,且对人体无害.下列说法正确的是( )
| A. | 氯气的化学式为 Cl | |
| B. | HClO 杀菌消毒是化学变化 | |
| C. | 高铁酸钠是氧化物 | |
| D. | 用高铁酸钠净化生产的自来水是纯净物 |