题目内容
(题文)我国高纯氧化镁产品供不应求,工业上可以用硫酸镁还原热解制备,工业流程如下:
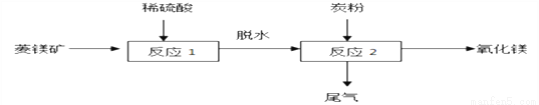
(1)菱镁矿主要成分是碳酸镁,反应前要粉粹,目的是________,反应1化学反应方程式为________。
(2)反应2中的化学方程式为:2MgSO4+C 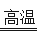 2MgO+2SO2↑+________。
2MgO+2SO2↑+________。
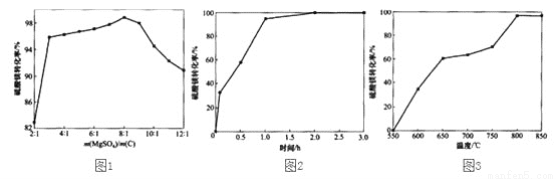
(3)反应2中硫酸镁与炭的配比对硫酸镁转化率的影响如下图1,硫酸镁转化率最高时m(MgSO4):m(C)=________,当配炭比2:1~3:1时硫酸镁转化率低的原因是________。
(4)反应2中时间和温度对硫酸镁转化率的影响分别如下图2、图3,则最佳的时间和温度分别为_____h、____℃。
(5)尾气直接排放到空气中会引起________、________两个当今世界全球性问题,可以用石灰浆吸收其中的有毒气体,化学方程式为:________。
增大接触面积,充分反应MgCO3+H2SO4═MgSO4+H2O+CO2↑CO2↑8:1炭粉较多,硫酸镁被炭粉包裹,受热面积小,传热性降低2h800℃温室效应酸雨SO2+Ca(OH)2=CaSO3+H2O 【解析】 (1)反应物的接触面积越大,反应速率越快;碳酸镁与硫酸反应生成硫酸镁、二氧化碳气体和水,据此写出反应的化学方程式; (2)根据质量守恒定律分析解答; (3)根据...
练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目



 2Fe203
2Fe203