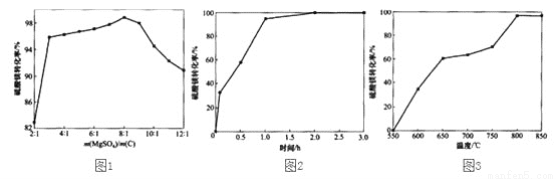
��Ŀ����
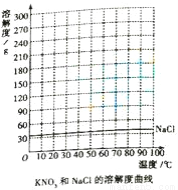
��ͼ������β���������з�����һ����Ӧ����ʾ��ͼ�����С���ʾ̼ԭ�ӡ����𡱱�ʾ��ԭ�ӡ�����ɫԲȦ����ʾ��ԭ�ӣ������й�˵��������ǣ� ��

A. ���ɵ����ʶ�����������ɿ���������
B. ��Ӧǰ��ԭ�ӵ������
C. �÷�Ӧ���ڻ��Ϸ�Ӧ
D. ��Ӧǰ��������Ԫ�صĻ��ϼ۷����˱仯
C �������� ������ͼ��֪������Ϊ�����Ͷ�����̼���ǿ����й��еijɷ֣���Ӧǰ��ԭ�ӵ�����������䣻�����ֻ�����������������һ�����ʵķ�Ӧ�л��Ϸ�Ӧ����Ӧǰ����Ԫ�صĻ��ϼ۶�Ϊ-2�ۣ�û�иı䣻ij��ѧС��������ϳ���̽������֪�����ȵ�����غ��Ȼ��ƵĻ�������ᴿ����ء���
�������ᴿ������
��һ�������£�20�棩�ܽ�Ⱥ��ܽ��ԵĹ�ϵ
�ܽ��S | S��10g | 1g��S��10g | 0.01g��S��1g | S��0.01g |
�ܽ��� | ���� | ���� | �� | ���� |
����������غ��Ȼ����ڲ�ͬ�¶�ʱ���ܽ��
�¶�/�� | 0 | 20 | 40 | 60 | 80 | 100 | |
�ܽ��/g | KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
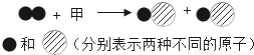
��1���ٳ����£�KNO3��NaCl���ܽ��Ծ�Ϊ______��
�ڸ��ݱ������ݣ�����KNO3���ܽ������_____��
�۸���KNO3���ܽ�����ߣ����KNO3��70��ʱ���ܽ��ԼΪ ______g��
��2��������ᴿ���裩
��ѡȡ��Ʒ��95gKNO3��5gNaCl�Ļ���
������80��ʱKNO3�ı�����Һ����ˮԼ56.2mL��ˮ���ܶ�ԼΪ1g•mL��1��
�۽�����20��
�ܵõ�����
������ᴿ������
Ϊ��֤�����еõ��ľ���Ϊ������KNO3����С��ͬѧ�������֪ʶ���������ϳ�����������·������������Dz�ͬ���ʶ��ܽ�ȵ��Ӱ�켰ʵ�������ˮ���������ʧ��Ӱ�����أ�
����һ ͨ����ѧʵ����м��飬ȡ������4���еõ��ľ������Թ��У���ˮ�����Һ���μ�________���۲�ʵ������
������ ��������KNO3���������ԼΪ________g����ȷ��0.1g���루4���еõ�������������бȽϣ�
������________��95%���бȽϣ�
������________��
����138������77.282%����20.2g��5g���бȽ� �������� ��1�����ɱ�����֪��20��ʱ��NaCl��KNO3���ܽ�ȷֱ�Ϊ31.6g��36.0g��������10g�����Գ����£�KNO3��NaCl���ܽ��Ծ�Ϊ���ܣ� �ڸ��ݱ�����������ڲ�ͬ�¶��µ��ܽ�ȣ��ú������ʾ�¶ȣ��������ʾ���ʵ��ܽ�ȣ��ɻ������ܽ�����ߣ� �������Ƶ����ߣ��ҳ�KNO3�����к�����Ϊ70ʱ����...

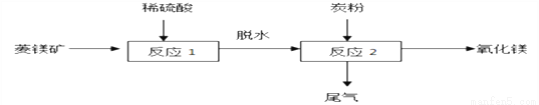
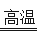 2MgO+2SO2��+________��
2MgO+2SO2��+________��