题目内容
(6分)某环保小组监测到一湿法冶铜厂排放的废水中含有硫酸和硫酸铜两种污染物,为测定该废水中各污染物的含量,给冶铜厂提供处理废水的参考,环保小组的同学进行了以下实验。取废水500g,向其中加入溶质质量分数为20%的氢氧化钠溶液。测得沉淀质量与所加入的氢氧化钠溶液的质量关系如下图:
根据所得数据计算:
(1)500g该废水中硫酸铜的质量。
(2)该废水中硫酸的溶质质量分数。
(6分)解:设500g废水中CuSO4的质量为χ,与CuSO4反应的NaOH溶液的质量为y,500g该废水中H2SO4的质量为z。
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4(1分)
160 80 98
χ y×20% 19.6g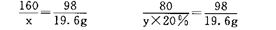
χ=32g(1分) y=80g(1分)
H2SO4+2NaOH=Na2SO4+2H2O(1分)
98 80
z (120g一80g)×20%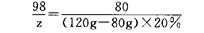
z=9.8g(1分)
废水中硫酸的质量分数为9.8/500g×100%=1.96%(1分)
答:500g该废水中CuSO4的质量是32g,该废水中硫酸的质量分数为1.96%。
解析

练习册系列答案
相关题目


