题目内容
15.下列物质的应用时,应用其物理性质的是( )
| A. | ②④ | B. | ④ | C. | ①②④ | D. | ①②③ |
分析 根据物质的性质进行分析,氢氧化镁具有碱性,能与酸反应,盐酸能与氧化铁反应,大理石硬度大,能用作建筑材料,熟石灰具有碱性,常用于改良酸性土壤.
解答 解:①氢氧化镁具有碱性,能和盐酸反应,利用了其化学性质,故①错误;
②氮气用于食品防腐--利用了氮气的化学性质不活泼,利用了其化学性质,故②错误;
③氧气用于气焊,是利用了氧气能支持燃烧的性质,需要通过化学变化才表现出来,是利用了其化学性质,故③错误;
④稀有气体用作霓虹灯,不需要发生化学变化就能表现出来,是利用了其物理性质,故④正确;
故选B.
点评 本题主要考查了物质用途,完成此题,可以依据物质的性质进行.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
5.下列对实验现象描述中,正确的是( )
| A. | 镁带在空气中燃烧发出耀眼强光 | B. | 木炭在O2中燃烧火星四射 | ||
| C. | 硫在O2燃烧发出淡蓝色火焰 | D. | 红磷在空气中燃烧产生白雾 |
6.在电解水的实验中可以直接观察到的现象是( )
| A. | 水是由氢元素和氧元素组成的 | B. | 在两个电极上均有无色气泡产生 | ||
| C. | 有氢气和氧气产生,质量比为2:1 | D. | 水分子由氢原子和氧原子构成的 |
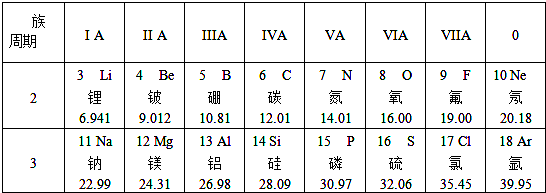
20. 根据图中的信息判断,下列说法错误的是( )
根据图中的信息判断,下列说法错误的是( )
 根据图中的信息判断,下列说法错误的是( )
根据图中的信息判断,下列说法错误的是( )| A. | 硫原子的质子数是16 | B. | 硫原子核外有3个电子层 | ||
| C. | 当X=8时,该微粒是阳离子 | D. | 在化学变化中,硫原子易得电子 |
7.三甲基一氯硅烷【(CH3)3SiCl】是一种生产有机硅化合物的原料,遇明火会引起爆炸,在空气中燃烧生成一氧化碳、二氧化碳、二氧化硅和氯化氢,三甲基一氯硅烷与水接触可产生雾状盐酸.则下列说法正确的是( )
| A. | 保存三甲基一氯硅烷时应密封防水 | |
| B. | 三甲基一氯硅烷遇明火引起的爆炸属于物理变化 | |
| C. | 扑灭三甲基一氯硅烷引发着火,应使用高压水枪 | |
| D. | 三甲基一氯硅烷由碳、氢、硅、氯四种原子构成 |
4. 右图中甲、乙、丙、丁、戊形成了“奥运五环”,且相连两个环对应的物质(或其溶液)在常温条件下能发生化学反应.其中甲、乙、丙、丁是CuSO4、Fe、H2SO4和CuO中的一种.若丙为单质,则戊可能是下列哪种物质( )
右图中甲、乙、丙、丁、戊形成了“奥运五环”,且相连两个环对应的物质(或其溶液)在常温条件下能发生化学反应.其中甲、乙、丙、丁是CuSO4、Fe、H2SO4和CuO中的一种.若丙为单质,则戊可能是下列哪种物质( )
 右图中甲、乙、丙、丁、戊形成了“奥运五环”,且相连两个环对应的物质(或其溶液)在常温条件下能发生化学反应.其中甲、乙、丙、丁是CuSO4、Fe、H2SO4和CuO中的一种.若丙为单质,则戊可能是下列哪种物质( )
右图中甲、乙、丙、丁、戊形成了“奥运五环”,且相连两个环对应的物质(或其溶液)在常温条件下能发生化学反应.其中甲、乙、丙、丁是CuSO4、Fe、H2SO4和CuO中的一种.若丙为单质,则戊可能是下列哪种物质( )| A. | HCl | B. | NaOH | C. | NaCl | D. | Cu |
5.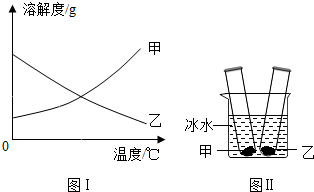 甲、乙两种固体物质的溶解度曲线如图Ⅰ所示.常温下,分别向装有适量甲、乙物质的两支试管里加入等量的蒸馏水,充分振荡后,两支试管底部均有未溶解的固体;再将两支试管放入盛有冰水混合物的烧杯里,如图Ⅱ所示.关于该实验,下列说法中正确的是( )
甲、乙两种固体物质的溶解度曲线如图Ⅰ所示.常温下,分别向装有适量甲、乙物质的两支试管里加入等量的蒸馏水,充分振荡后,两支试管底部均有未溶解的固体;再将两支试管放入盛有冰水混合物的烧杯里,如图Ⅱ所示.关于该实验,下列说法中正确的是( )
 甲、乙两种固体物质的溶解度曲线如图Ⅰ所示.常温下,分别向装有适量甲、乙物质的两支试管里加入等量的蒸馏水,充分振荡后,两支试管底部均有未溶解的固体;再将两支试管放入盛有冰水混合物的烧杯里,如图Ⅱ所示.关于该实验,下列说法中正确的是( )
甲、乙两种固体物质的溶解度曲线如图Ⅰ所示.常温下,分别向装有适量甲、乙物质的两支试管里加入等量的蒸馏水,充分振荡后,两支试管底部均有未溶解的固体;再将两支试管放入盛有冰水混合物的烧杯里,如图Ⅱ所示.关于该实验,下列说法中正确的是( )| A. | 甲、乙两物质的溶解度都增大 | |
| B. | 两支试管里剩余的固体都增多 | |
| C. | 乙溶液中溶质的质量分数增大 | |
| D. | 装有甲物质的试管中剩余的固体减少 |
 (1)用化学符号表示:
(1)用化学符号表示: