题目内容
小明同学在父亲的工厂里,看见厂里进来的纯碱包装袋上的说明如图.他想探究该纯碱的含量与说明是否相符,就在厂里的化验室进行有关实验:他用天平准确称取纯碱样品11g,放入质量为20g的烧杯中,逐渐加入某浓度的盐酸,边加边搅拌,加到不再产生气体为止,用去盐酸73g,再用天平称量反应后的烧杯和溶液,总质量为99.6g.试计算:(1)反应中产生二氧化碳气体______克?
(2)请你帮他计算(写出计算过程),据计算结果判断该纯碱纯度是否与说明相符?

【答案】分析:(1)根据质量守恒定律结合题中反应前后物质质量的变化可以求算出生成二氧化碳的质量;
(2)根据生成二氧化碳的质量结合化学方程式可以求算出碳酸钠的质量,然后计算出纯碱的纯度与题中的标签比较可以作出判断.
解答:解:(1)根据质量守恒定律可以知道生成二氧化碳的质量为:11g+20g+73g-99.6g=4.4g;
(2)设纯碱样品中含碳酸钠的质量为x
Na2CO3+2HCl═2 NaCl+H2O+CO2↑
106 44
x 4.4g

x=l0.6g;
样品中Na2CO3的质量分数为: ×100%=96.4%
×100%=96.4%
因为Na2CO3的质量分数96.4%>95%,所以该纯碱纯度与说明相符.
答:该纯碱纯度与说明相符.
故答案为:(1)4.4;
(2)该纯碱纯度与说明相符.
点评:此题是对化学方程式计算的考查,解题的关键是找到已知量,此题则是利用反应前后物质的质量的变化求出生成二氧化碳的质量,而后根据它的质量求出其它的需要的物质的质量解答即可.
(2)根据生成二氧化碳的质量结合化学方程式可以求算出碳酸钠的质量,然后计算出纯碱的纯度与题中的标签比较可以作出判断.
解答:解:(1)根据质量守恒定律可以知道生成二氧化碳的质量为:11g+20g+73g-99.6g=4.4g;
(2)设纯碱样品中含碳酸钠的质量为x
Na2CO3+2HCl═2 NaCl+H2O+CO2↑
106 44
x 4.4g

x=l0.6g;
样品中Na2CO3的质量分数为:
 ×100%=96.4%
×100%=96.4%因为Na2CO3的质量分数96.4%>95%,所以该纯碱纯度与说明相符.
答:该纯碱纯度与说明相符.
故答案为:(1)4.4;
(2)该纯碱纯度与说明相符.
点评:此题是对化学方程式计算的考查,解题的关键是找到已知量,此题则是利用反应前后物质的质量的变化求出生成二氧化碳的质量,而后根据它的质量求出其它的需要的物质的质量解答即可.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
 (2006?湘西州)小明同学在父亲的工厂里,看见厂里进来的纯碱包装袋上的说明如图.他想探究该纯碱的含量与说明是否相符,就在厂里的化验室进行有关实验:他用天平准确称取纯碱样品11g,放入质量为20g的烧杯中,逐渐加入某浓度的盐酸,边加边搅拌,加到不再产生气体为止,用去盐酸73g,再用天平称量反应后的烧杯和溶液,总质量为99.6g.试计算:
(2006?湘西州)小明同学在父亲的工厂里,看见厂里进来的纯碱包装袋上的说明如图.他想探究该纯碱的含量与说明是否相符,就在厂里的化验室进行有关实验:他用天平准确称取纯碱样品11g,放入质量为20g的烧杯中,逐渐加入某浓度的盐酸,边加边搅拌,加到不再产生气体为止,用去盐酸73g,再用天平称量反应后的烧杯和溶液,总质量为99.6g.试计算:
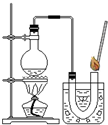 小明同学在家里的药箱中发现一瓶用来清洗伤口用的消毒液--“双氧水”,他联想到在化学课上曾用过氧化氢溶液制取过氧气,他高兴的将家中的“双氧水”拿到学校的实验室,在老师的指导下和同学们一起做了如下实验.
小明同学在家里的药箱中发现一瓶用来清洗伤口用的消毒液--“双氧水”,他联想到在化学课上曾用过氧化氢溶液制取过氧气,他高兴的将家中的“双氧水”拿到学校的实验室,在老师的指导下和同学们一起做了如下实验. 小明同学在父亲的工厂里,看见厂里进来的纯碱包装袋上的说明如图.他想探究该纯碱的含量与说明是否相符,就在厂里的化验室进行有关实验:他用天平准确称取纯碱样品11g,放入质量为20g的烧杯中,逐渐加入某浓度的盐酸,边加边搅拌,加到不再产生气体为止,用去盐酸73g,再用天平称量反应后的烧杯和溶液,总质量为99.6g.试计算:
小明同学在父亲的工厂里,看见厂里进来的纯碱包装袋上的说明如图.他想探究该纯碱的含量与说明是否相符,就在厂里的化验室进行有关实验:他用天平准确称取纯碱样品11g,放入质量为20g的烧杯中,逐渐加入某浓度的盐酸,边加边搅拌,加到不再产生气体为止,用去盐酸73g,再用天平称量反应后的烧杯和溶液,总质量为99.6g.试计算: