题目内容
由钠和铝构成的合金共 m g,放入适量水中充分反应(没有固体剩余)共产生 n L(标况)气体,试求合金中钠和铝的质量各是多少克?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据钠遇水反应2Na+2H2O═2NaOH+H2↑,铝与氢氧化钠的反应2Al+2NaOH+6H2O═2 Na[Al(OH)4]+3 H2↑,由生成氢气的体积计算解答.
解答:解:设该合金中钠和铝的质量分别为:m(Na)、m(Al),发生的反应为:2Na+2H2O═2NaOH+H2↑
2Al+2NaOH+6H2O═2 Na[Al(OH)4]+3 H2↑
m(Na)+m(Al)=m g
m(Na)/23 g?mol-1×1/2×22.4L?mol-1+m(Al)/27 g?mol-1×2/3×22.4L?mol-1=n L
解得:m(Na)=(1.64m-1.32n) g
m(Al)=(1.32n-0.64m) g
答案:合金中钠的质量=(1.64m-1.32n) g
合金中铝的质量(1.32n-0.64m) g
2Al+2NaOH+6H2O═2 Na[Al(OH)4]+3 H2↑
m(Na)+m(Al)=m g
m(Na)/23 g?mol-1×1/2×22.4L?mol-1+m(Al)/27 g?mol-1×2/3×22.4L?mol-1=n L
解得:m(Na)=(1.64m-1.32n) g
m(Al)=(1.32n-0.64m) g
答案:合金中钠的质量=(1.64m-1.32n) g
合金中铝的质量(1.32n-0.64m) g
点评:本题考查混合物有关计算,难度较大,侧重对基础知识的巩固,注意掌握根据方程式的计算.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目

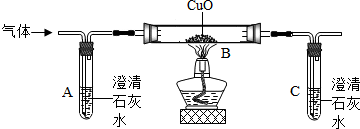 不少同学都被蚊虫叮咬过,感觉又痛又痒.同学们从化学课上知道:蚊虫叮咬时能在人的皮肤内分泌出蚁酸刺激皮肤.课外兴趣小组同学决定对蚁酸进行探究.
不少同学都被蚊虫叮咬过,感觉又痛又痒.同学们从化学课上知道:蚊虫叮咬时能在人的皮肤内分泌出蚁酸刺激皮肤.课外兴趣小组同学决定对蚁酸进行探究.