题目内容
12.现有10碳酸钙与100克稀盐酸恰好完全反应,求反应后溶液中溶质的质量分数.分析 根据反应后生成物溶液的溶质是氯化钙,质量可由碳酸钙的质量求得,根据质量守恒定律,反应后溶液质量是反应前总质量减去生成的二氧化碳质量,即为溶液的质量,然后求出其质量分数即可.
解答 解:(1)设生成二氧化碳的质量为y,反应后生成氯化钙的质量为z,
CaCO3 +2HCl═CaCl2 +CO2↑+H20
100 73 111 44
10g z y
$\frac{100}{10g}$=$\frac{111}{z}$=$\frac{44}{y}$
y=4.4g
z=11.1g
所以反应后溶液中溶质的质量分数为:$\frac{11.1g}{10g+100g-4.4g}$×100%=10.5%.
故答案为:反应后溶液中溶质质量分数为:10.5%.
点评 根据化学方程式进行计算时,只能使用纯净物的质量进行计算,而不能把混合物的质量直接代入化学方程式进行计算.

练习册系列答案
相关题目
2.用图1和图2所示装置分别制取适量氧气和二氧化碳气体,请回答下列问题:
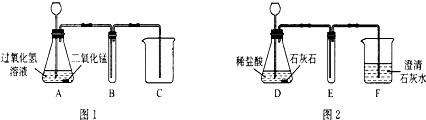
(1)A中长颈漏斗伸入液面下是为了防止气体从漏斗中逸出.
(2)写出A、D中发生反应的文字表达式:A中过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;D中盐酸+碳酸钙-→氯化钙+水+二氧化碳.
(3)按实验要求完成下表内容(有斜线处不需要填):

(1)A中长颈漏斗伸入液面下是为了防止气体从漏斗中逸出.
(2)写出A、D中发生反应的文字表达式:A中过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;D中盐酸+碳酸钙-→氯化钙+水+二氧化碳.
(3)按实验要求完成下表内容(有斜线处不需要填):
| 制取气体 | 应加入的物质名称 | 物质或装置所起的作用 | |
| 氧气 | B | 水 | 收集氧气 |
| C |  | 收集排出的水 | |
| 二氧化碳 | E |  | 收集二氧化碳 |
| F | 澄清石灰水 | 检验二氧化碳是否集满 | |
4.下列化合物中,氮元素的质量分数最小的是( )
| A. | NH4Cl | B. | NH4NO3 | C. | CO(NH2)2 | D. | (NH4)2SO4 |
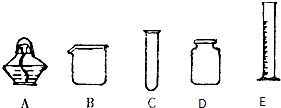 如图仪器中,既能用来配制溶液又能作较大量试剂反应容器的是(填标号)B,用作收集或贮存少量气体的是D,可间接加热的仪器是B,A仪器的名称是酒精灯.
如图仪器中,既能用来配制溶液又能作较大量试剂反应容器的是(填标号)B,用作收集或贮存少量气体的是D,可间接加热的仪器是B,A仪器的名称是酒精灯.