题目内容
2. 如图表示两种物质发生的化学反应,其中相同的球代表同种原子,小球间的短线代表原子间的结合.下列说法中不正确的是( )
如图表示两种物质发生的化学反应,其中相同的球代表同种原子,小球间的短线代表原子间的结合.下列说法中不正确的是( )| A. | 图示有4种分子 | B. | 图示反应前后原子个数不变 | ||
| C. | 图示发生了化合反应 | D. | 图示产物为混合物 |
分析 A、观察微粒的微观构成,判断分子的种类;
B、根据反应前后原子的种类、数目分析;
C、根据化合反应的生成物的特点分析;
D、根据微粒的构成,分析物质种类.
解答 解:A、由微观模型示意图可知,图示中共有4种不同的分子构成,有4种分子.故A正确;
B、对比反应前后微粒的变化可知,原子的种类、数目不变.故B正确;
C、由该反应的生成物的微观模型示意图可知,反应物为一种化合物一种单质,生成物为两种化合物;该反应不属于化合反应.故不正确;
D、由微粒的变化可知.生成物中有两种化合物,是混合物.故D正确.
故选C.
点评 分子由原子构成,构成不同的分子属于不同种物质的分子,由同种原子构成的分子属于单质分子,由不同种原子构成的分子属于化合物的分子.

练习册系列答案
相关题目
5.下列是生活中常见的一些现象,其中属于化学变化的是( )
| A. | 石蜡熔化 | B. | 瓷碗破碎 | ||
| C. | 潮湿的衣服被晒干了 | D. | 洗净的铁锅出现锈渍 |
2.下列有关实验现象的描述中,正确的是( )
| A. | 镁带在氧气中燃烧,产生黑烟 | |
| B. | 细铁丝在氧气中燃烧,火星四射,生成四氧化三铁固体 | |
| C. | 硫在空气中燃烧,发出蓝紫色火焰 | |
| D. | 蜡烛在盛氧气的集气瓶中燃烧,发出白光,瓶壁出现液雾 |
9.下列化学符号正确的是( )
| A. | 钠元素符号:NA | B. | 2个铝离子:2Al3+ | C. | 3个水分子:3HO2 | D. | 4个氢原子:2H2 |
11.下列检验方法正确的是( )
| A. | 检验溶液中的H+,加入AgNO3溶液,再加稀硝酸 | |
| B. | 检验溶液中的Cl-,先加硝酸钡溶液,再加AgNO3溶液 | |
| C. | 检验溶液中的SO42-,先加稀盐酸,再加BaCl2溶液 | |
| D. | 检验溶液中的SO42-,先加BaCl2溶液,再加稀盐酸 |
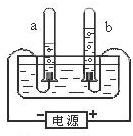 实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题:
实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题: 化学实验小组的同学们把盐酸和石灰石放入气密性良好的图装置中,
化学实验小组的同学们把盐酸和石灰石放入气密性良好的图装置中,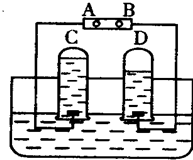 如图是电解水的简易装置.回答下列各问题:
如图是电解水的简易装置.回答下列各问题: