题目内容
5.10g氯酸钾与二氧化锰的混合物加热,完全反应后,质量减少3.2g,则原混合物中二氧化锰的质量是多少?分析 根据质量守恒定律,由反应前后固体减少的质量为反应放出氧气的质量;再利用产生氧气的质量计算参加反应的氯酸钾的质量,混合物质量与氯酸钾质量差即为二氧化锰的质量.
解答 解:根据质量守恒定律,反应放出氧气的质量为3.2g
设氯酸钾的质量为x
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 96
x 3.2g
$\frac{245}{x}=\frac{96}{3.2g}$
x=8.17g
原混合物中二氧化锰的质量=10g-8.17g=1.83g
答:原混合物中二氧化锰的质量是1.83g.
点评 由于二氧化锰在反应中为催化剂,反应前后质量不变,本题也可以由氧气质量计算反应生成氯化钾的质量,而由反应后固体求出二氧化锰的质量.

练习册系列答案
相关题目
15.下面是几种粒子的结构示意图:
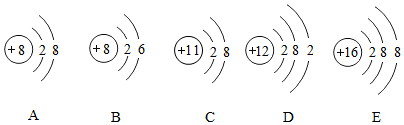
(1)A~E共有4种元素,B所表示的元素位于元素周期表的第2周期;
(2)表示原子的粒子有BD (填元素符号,下同);
(3)表示阴离子的有AE;
(4)表示阳离子的有C.

(1)A~E共有4种元素,B所表示的元素位于元素周期表的第2周期;
(2)表示原子的粒子有BD (填元素符号,下同);
(3)表示阴离子的有AE;
(4)表示阳离子的有C.
13.下列知识点归纳正确的是( )
| A. | 由同种元素组成的物质一定是单质 | |
| B. | 质子数相同的两种粒子一定属于同种元素 | |
| C. | 离子是带电的粒子,则带电的粒子一定是离子 | |
| D. | 在同一化合物中,同一元素可以显不同的化合价 |
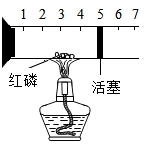 为测定空气中氧气的含量,某同学设计了如图所示实验装置.其中,右侧为可以自由移动的活塞(忽略摩擦力).装置的气密性完好,实验过程开始前右侧活塞位于刻度5处.
为测定空气中氧气的含量,某同学设计了如图所示实验装置.其中,右侧为可以自由移动的活塞(忽略摩擦力).装置的气密性完好,实验过程开始前右侧活塞位于刻度5处.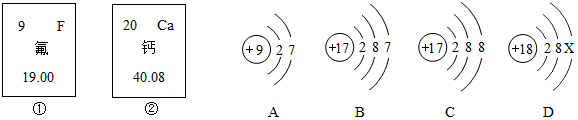
 .
.