题目内容
20.某无色气体可能含有H2、CO、CH4中的一种或几种,依次进行下列实验(假设每一步反应或吸收均完全):①无色气体在氧气中充分燃烧;②燃烧后生成的气体通过盛浓硫酸的装置,装置的质量增加;③再将剩余气体通过盛NaOH溶液的装置,装置的质量增加.下列推断正确的是:(提示:浓硫酸可吸收水分,NaOH溶液的性质与石灰水的相似)( )| A. | 该气体一定只含有H2 | B. | 该气体可能只含H2和CH4 | ||
| C. | 该气体可能只含CO | D. | 无法判断 |
分析 根据无色气体在氧气中充分燃烧,燃烧后生成的气体通过盛浓硫酸的装置,浓硫酸所增加的质量即气体燃烧生成水的质量,说明含有氢元素;再将剩余气体通过盛NaOH溶液的装置,增加的质量是吸收了生成气体中二氧化碳,因此气体中含有碳元素,结合三种气体的燃烧产物分析.
解答 解:无色气体在氧气中充分燃烧,燃烧后生成的气体通过盛浓硫酸的装置,浓硫酸所增加的质量即气体燃烧生成水的质量,说明含有氢元素;再将剩余气体通过盛NaOH溶液的装置,增加的质量是吸收了生成气体中二氧化碳,因此气体中含有碳元素,因此该气体可能是甲烷,也可能是甲烷和氢气或甲烷与一氧化碳或甲烷、一氧化碳和氢气,也可能是氢气和一氧化碳等多种情况,观察选项,A产物,B正确,C错误,D错误;故选项为:B.
点评 本题主要考查常见气体燃烧的产物以及根据产物判断物质,同学们一定要了解常见物质的性质.

练习册系列答案
 期末集结号系列答案
期末集结号系列答案
相关题目
15.对下列化学用语解释正确的是( )
| A. | Mg+--镁离子 | B. | O2--两个氧原子 | C. | 2H2--两个氢分子 | D. | 2N--两个氮元素 |
12.创建文明卫生城市,保护环境人人有责.下列措施有利于环境保护的是( )
①超市和商城等对塑料袋实行有偿使用
②倡导公共大交通,减少机动车燃油排放含氮、硫的氧化物的量
③在太湖流域的每个城市建设生活污水处理设施
④大量使用农药、化肥,以提高农作物产量
⑤露天焚烧处理生活垃圾和农作物秸秆.
①超市和商城等对塑料袋实行有偿使用
②倡导公共大交通,减少机动车燃油排放含氮、硫的氧化物的量
③在太湖流域的每个城市建设生活污水处理设施
④大量使用农药、化肥,以提高农作物产量
⑤露天焚烧处理生活垃圾和农作物秸秆.
| A. | ①②③ | B. | ②③④ | C. | ①②③④ | D. | ①②③④⑤ |
9.下列各组物质可以按照指定顺序进行直接转化的是( )
| A. | S→SO2→Na2SO4→NaOH | B. | HCl→NaCl→CaCl2→HCl | ||
| C. | CO2→Na2CO3→CaCO3→CO2 | D. | Fe→Fe2O3→FeSO4→Fe |
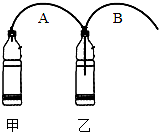 如图所示,有人制作了一个家庭制氧装置.该制氧装置由2个饮料瓶、2根软管和药剂构成,整套装置成本不到3块钱.药剂包括过氧碳酸钠(2Na2CO3•3H2O2)和二氧化锰.制氧时,先在两个饮料瓶中加入适量的水,再往甲瓶中加入药剂,产生的气体通过B管从乙瓶导出,即可供人吸氧.
如图所示,有人制作了一个家庭制氧装置.该制氧装置由2个饮料瓶、2根软管和药剂构成,整套装置成本不到3块钱.药剂包括过氧碳酸钠(2Na2CO3•3H2O2)和二氧化锰.制氧时,先在两个饮料瓶中加入适量的水,再往甲瓶中加入药剂,产生的气体通过B管从乙瓶导出,即可供人吸氧. 如图是化肥尿素标签上的部分文字说明.请回答下列问题:
如图是化肥尿素标签上的部分文字说明.请回答下列问题: