题目内容
15.我国自主研发的药物帕拉米韦(化学式为C15H20N4O4)可用于治疗H7N9禽流感,下列关于帕拉米韦的说法正确的是( )| A. | 含有2个氧分子 | B. | 碳元素与氮元素的质量比为15:24 | ||
| C. | 属于无机物 | D. | 相对分子质量为328 |
分析 A、根据帕拉米韦的微观构成,进行分析判断.
B、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
C、根据含有碳元素的化合物叫有机化合物,简称有机物,进行分析判断.
D、根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析判断.
解答 解:A、帕拉米韦是由帕拉米韦分子构成的,不含氧分子,故选项说法错误.
B、碳元素与氮元素的质量比为(12×15):(14×4)≠15:24,故选项说法错误.
C、帕拉米韦是含碳元素的化合物,属于有机物,故选项说法错误.
D、相对分子质量为12×15+1×28+14×4+16×4=328,故选项说法正确.
故选:D.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
5. 小红发现实验台上有两瓶标签破损的无色溶液(如图所示),询问老师,确认溶液是初中化学实验用剩的两种化学试剂.于是她对溶液的成分进行了以下探究.
小红发现实验台上有两瓶标签破损的无色溶液(如图所示),询问老师,确认溶液是初中化学实验用剩的两种化学试剂.于是她对溶液的成分进行了以下探究.
【提出问题】这两瓶试剂分别是什么?
【作出猜想】可能是NaOH溶液、Na2CO3溶液、NaHCO3溶液、NaCl溶液、Na2SO4溶液中的任意两种.
【查阅资料】①Na2CO3溶液、NaHCO3溶液呈碱性,NaCl溶液、Na2SO4溶液呈中性;
②碳酸氢钙可溶于水;
③2NaHCO3+Ca(OH)2═CaCO3↓+Na2CO3+2H2O
【设计方案并进行实验】分别取少量瓶中溶液进行以下实验;
【实验反思】小红经过分析认为1号溶液还可能是变质的氢氧化钠溶液,写出氢氧化钠溶液变质的化学方程式2NaOH+CO2═Na2CO3+H2O.
 小红发现实验台上有两瓶标签破损的无色溶液(如图所示),询问老师,确认溶液是初中化学实验用剩的两种化学试剂.于是她对溶液的成分进行了以下探究.
小红发现实验台上有两瓶标签破损的无色溶液(如图所示),询问老师,确认溶液是初中化学实验用剩的两种化学试剂.于是她对溶液的成分进行了以下探究.【提出问题】这两瓶试剂分别是什么?
【作出猜想】可能是NaOH溶液、Na2CO3溶液、NaHCO3溶液、NaCl溶液、Na2SO4溶液中的任意两种.
【查阅资料】①Na2CO3溶液、NaHCO3溶液呈碱性,NaCl溶液、Na2SO4溶液呈中性;
②碳酸氢钙可溶于水;
③2NaHCO3+Ca(OH)2═CaCO3↓+Na2CO3+2H2O
【设计方案并进行实验】分别取少量瓶中溶液进行以下实验;
| 实验步骤 | 实验现象 | 实验结论 |
实验1:分别测定两种溶液的pH 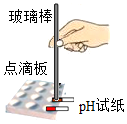 | 两种溶液的pH均大于7 | 两瓶溶液一定不是NaCl溶液、Na2SO4溶液 |
实验2: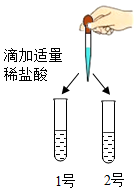 | 均有气泡产生 | 两瓶溶液分别是NaHCO3溶液和Na2CO3溶液.写出Na2CO3溶液与盐酸反应的化学方程式Na2CO3+2HCl═2NaCl+H2O+CO2↑. |
实验3:滴加适量氯化钙溶液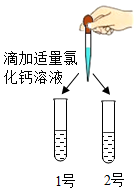 | 1号试管中出现白色沉淀,2号试管中无明显现象 | 1号溶液是Na2CO3溶液 2号溶液是NaHCO3溶液. |
3.逻辑推理是一种重要的化学思维方法,下列推理不合理的是( )
| A. | 有些金属与酸反应产生气体,但与酸反应产生气体的不一定是金属 | |
| B. | 酸的组成中含有氢元素,但含有氢元素的化合物不一定是酸 | |
| C. | 化学变化中分子发生改变,但分子发生改变的变化不一定是化学变化 | |
| D. | 离子是带电的原子或原子团,但带电的粒子不一定是离子 |
4.金属钛(Ti)抗腐蚀性能好,露置于空气中数年,仍光亮如初,以金红石(主要成分是TiO2)为原料生产金属钛的步骤主要有:①在高温下,向金红石与焦炭的混合物中通入氯气(Cl2),得到TiCl4和一种可燃性气体;②在稀有气体环境和加热条件下,用Mg和TiCl4反应得到Ti和MgCl2,下列说法正确的是( )
| A. | ①中的反应TiO2+C+2Cl2$\frac{\underline{\;高温\;}}{\;}$TiCl4+CO2 | |
| B. | ②中的稀有气体的作用是隔绝空气 | |
| C. | ②中发生的反应为置换反应 | |
| D. | 金属钛在常温下易与O2反应 |
 江西省各地的共享单车方便了人们的出行,作为常用的代步工具,既轻便灵活,又符合环保要求.如图是一款共享单车的示意图.
江西省各地的共享单车方便了人们的出行,作为常用的代步工具,既轻便灵活,又符合环保要求.如图是一款共享单车的示意图.