题目内容
19. 小明在实验室发现一瓶未知溶质质量分数的氯化铜溶液.为了测定其溶质质量分数,他取出100克该溶液,向其中逐滴加入溶质质量分数为10%的氢氧化钠溶液.反应过程中生成沉淀的质量与所用氢氧化钠溶液质量关系如图所示.
小明在实验室发现一瓶未知溶质质量分数的氯化铜溶液.为了测定其溶质质量分数,他取出100克该溶液,向其中逐滴加入溶质质量分数为10%的氢氧化钠溶液.反应过程中生成沉淀的质量与所用氢氧化钠溶液质量关系如图所示.(1)两者刚好完全反应时,所加氢氧化钠溶液质量是80克.
(2)该氯化铜溶液的溶质质量分数是多少?
(反应的方程式为:CuCl2+2NaOH=Cu(OH)2↓+2NaCl)
分析 氯化铜和氢氧化钠反应生成氢氧化铜沉淀和氯化钠,根据反应的化学方程式及其提供的数据可以进行相关方面的计算.
解答 解:(1)两者刚好完全反应时,所加氢氧化钠溶液质量是80g.
故填:80.
(2)设氯化铜质量为x,
CuCl2+2NaOH=Cu(OH)2↓+2NaCl,
135 80
x 80g×10%
$\frac{135}{x}$=$\frac{80}{80g×10%}$,
x=13.5g,
该氯化铜溶液的溶质质量分数是:$\frac{13.5g}{100g}$×100%=13.5%,
答:该氯化铜溶液的溶质质量分数是13.5%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.下列实验事实不成立的是( )
| A. | 用酚酞溶液可鉴别稀盐酸、氢氧化钠溶液和氯化钠溶液 | |
| B. | 除去炭粉中混有的少量氧化铜粉末,可加足量稀硫酸后过滤 | |
| C. | Ba2+、OH-、NO3-、Na+四种离子在溶液中可以同时存在 | |
| D. | 分离氯化钠和碳酸钠两种固体,先加适量的稀盐酸,再蒸发 |
14.青色的虾、蟹煮熟后颜色会变成红色.小明认为这些生物体内含有的某种物质可能就像科学课上的酸碱指示剂一样,不同条件下颜色会发生改变.小明同学的看法属于科学探究中的( )
| A. | 实验 | B. | 假设 | C. | 观察 | D. | 下结论 |
4.在一密闭容器内加入A、B、C、D四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化见下表.下列说法中不正确的是( )
| 物质 | A | B | C | D |
| 反应前物质质量/g | 8 | 32 | 5 | 4 |
| 反应后物质质量/g | 16 | 4 | x | 24 |
| A. | 该反应为分解反应 | |
| B. | B、D两种物质间反应的质量比为7:5 | |
| C. | C可能为该反应的催化剂 | |
| D. | A、B两种物质间参加反应的质量比为1:4 |
17.化学是一门以实验为基础的科学,化学所取得的丰硕成果,是与实验的重要作用分不开的.结合下列实验装置图回答问题:
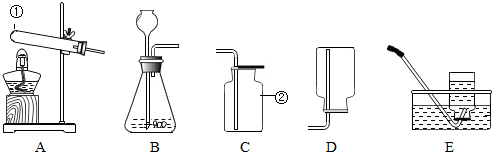
(1)写出指定仪器的名称:①试管 ②集气瓶
(2)实验室用高锰酸钾制取氧气时,在试管口要放一团棉花,原因是为了防止高锰酸钾粉末进入导管,可选用的发生装置是A(填编号),收集装置可选择E,理由是氧气不易溶于水,该反应的文字表达式是高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气.
(3)如果用排空气法收集氧气,验满的方法是将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了.
(4)检查B装置气密性时,用止水夹夹紧橡皮管,从长颈漏斗中倒入水至淹没下端管口,使长颈漏斗中形成一段水柱,过一会儿,水柱不下降证明气密性良好.
(5)查阅资料回答问题:
①制取氯气不可以采用装置A的理由是浓盐酸是液体.
②制取氯气不可以(填“可以”或“不可以”)采用装置B,理由是二氧化锰固体和浓盐酸制氯气需要加热.

(1)写出指定仪器的名称:①试管 ②集气瓶
(2)实验室用高锰酸钾制取氧气时,在试管口要放一团棉花,原因是为了防止高锰酸钾粉末进入导管,可选用的发生装置是A(填编号),收集装置可选择E,理由是氧气不易溶于水,该反应的文字表达式是高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气.
(3)如果用排空气法收集氧气,验满的方法是将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了.
(4)检查B装置气密性时,用止水夹夹紧橡皮管,从长颈漏斗中倒入水至淹没下端管口,使长颈漏斗中形成一段水柱,过一会儿,水柱不下降证明气密性良好.
(5)查阅资料回答问题:
| 物质 | 制取气体的药品 | 反应条件 | 气体的物理性质 |
| 氯气 | 二氧化锰固体和浓盐酸 | 加热 | 可溶于水,密度比空气大 |
②制取氯气不可以(填“可以”或“不可以”)采用装置B,理由是二氧化锰固体和浓盐酸制氯气需要加热.
18.俗话说:“万物生长靠太阳,植物生长靠营养”.当作物叶色淡黄,生长不茂盛时需要施用下列哪一种肥料( )
| A. | 硫酸镁 | B. | 氯化钾 | C. | 磷酸钙 | D. | 碳酸氢铵 |