题目内容
5.结合如图装置,回答有关问题:
(1)写出仪器①的名称长颈漏斗.
(2)某同学选择A装置制取氧气,其反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,实验过程中发现反应很剧烈,不易控制,为了得到平稳的氧气流,可把装置A中的仪器①更换为分液漏斗.实验室用加热氯化铵和氢氧化钙固体混合物的方法制取氨气,则选择的发生装置为B,写出该反应的化学方程式2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.
(3)实验室用石灰石和稀盐酸反应制取二氧化碳的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑,请在上图虚线框中画出收集二氧化碳的简易装置图.制得的二氧化碳气体中常含有氯化氢等少量杂质,为了得到纯净、干燥的CO2,除杂装置C和D的导管按气流方向连接顺序是C(选填字母);
A.d→e→f→g B.e→d→f→g C.f→g→d→e D.g→f→e→d
用化学反应方程式表示D中饱和NaHCO3溶液的作用NaHCO3+HCl=NaCl+H2O+CO2↑.
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据过氧化氢在二氧化锰的催化作用下生成水和氧气,分液漏斗可以控制液体的滴加速度,实验室制取氨气的反应物是固体,反应条件是加热,氢氧化钙和氯化铵在加热的条件下生成氯化钙、水和氨气进行分析;
(3)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,二氧化碳的密度比空气大,易溶于水,洗气应该是长进短出,先除去氯化氢气体,再除去水蒸气进行分析;
(4)根据碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,①是长颈漏斗;
(2)过氧化氢在二氧化锰的催化作用下生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,分液漏斗可以控制液体的滴加速度,所以为了得到平稳的氧气流,可把装置A中的仪器①更换为分液漏斗,实验室制取氨气的反应物是固体,反应条件是加热,所以选择的发生装置为B,氢氧化钙和氯化铵在加热的条件下生成氯化钙、水和氨气,化学方程式为:2NH4Cl+Ca(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑;
(3)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑,二氧化碳的密度比空气大,易溶于水,所以收集装置是:
洗气应该是长进短出,先除去氯化氢气体,再除去水蒸气,所以除杂装置C和D的导管按气流方向连接顺序是f→g→d→e,故选:C;
(4)碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳,化学方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑.
故答案为:(1)长颈漏斗;
(2)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,分液漏斗,B,2NH4Cl+Ca(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑;
(3)CaCO3+2HCl═CaCl2+H2O+CO2↑, ,C;
,C;
(4)NaHCO3+HCl=NaCl+H2O+CO2↑.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

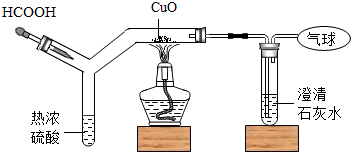 如图为CO还原CuO“微型”实验装置(夹持仪器等略),已知:HCOOH$\frac{\underline{\;热浓硫酸\;}}{\;}$H2O+CO↑,下列说法错误的是( )
如图为CO还原CuO“微型”实验装置(夹持仪器等略),已知:HCOOH$\frac{\underline{\;热浓硫酸\;}}{\;}$H2O+CO↑,下列说法错误的是( )| A. | 实验中所需CO可现制现用 | |
| B. | 此装置可节约用品,污染小,现象明显 | |
| C. | 此装置内空间较小,空气易排空,实验危险系数小 | |
| D. | 该实验中所涉及反应的基本类型有分解反应和置换反应 |
| A. |  向一定量的饱和石灰水中不断加入生石灰 | |
| B. |  向等质量的锌、铁中滴加等质量分数的稀盐酸 | |
| C. |  向一定量的氧化铁中通入一氧化碳气体并持续高温 | |
| D. |  向一定量的盐酸和氯化铜的混合溶液中滴加氢氧化钠溶液 |
| A. | 合金的熔点通常比组成它们的纯金属高 | |
| B. | 赤铁矿炼铁的主要原理:CO+FeO$\frac{\underline{\;高温\;}}{\;}$CO2+Fe | |
| C. | 用CuSO4溶液、Fe和Ag可以验证Fe、Cu、Ag三种金属的活动性强弱 | |
| D. | 铁制品生锈产生的铁锈主要成分是Fe3O4 |
(1)某地区学生营养午餐摄入标准值(每人每天)如表所示.
| 能量 | 3890kJ |
| 蛋白质 | 48g |
| 脂肪 | 30g |
| 钙 | 480mg |
| 锌 | 6mg |
| 铁 | 4mg |
| 维生素 | 24mg |
②人体不可缺少的营养物质有蛋白质、糖类、脂肪、维生素、水和矿物质;
(2)材料对我们生活的影响越来越大,下列属于合成材料的是bd.(填序号)
a.镁铝合金 b.聚乙烯 c.钢筋混凝土 d.有机玻璃.
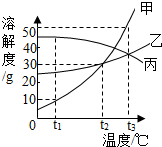 如图是甲、乙、丙三种固体物质在水中的溶解度曲线.下列说法不正确的是( )
如图是甲、乙、丙三种固体物质在水中的溶解度曲线.下列说法不正确的是( )| A. | t1℃时,甲、乙、丙溶解度大小顺序是丙>乙>甲 | |
| B. | t3℃时,将甲、乙饱和溶液降温至t2℃,所得溶液中溶质的质量分数相等 | |
| C. | t1℃时,将甲、丙饱和溶液恒温蒸发10g水后,前者析出晶体而后者无晶体析出 | |
| D. | t3℃时,8g甲中加20g水,充分溶解后再降温到t2℃,所得溶液为饱和溶液 |
 燃烧蚊香能将杀虫剂缓慢释放到空气中达到驱蚊效果.
燃烧蚊香能将杀虫剂缓慢释放到空气中达到驱蚊效果.