题目内容
5.下列相关事实用微观粒子的知识解释错误的是( )| 选项 | 事 实 | 解 释 |
| A | 用水银温度计测量体温 | 温度升高,分子间间隔变大 |
| B | 空气压缩可以变成液态空气 | 分子间有一定的间隔 |
| C | 冰水混合物属于纯净物 | 都含有同种分子 |
| D | 加热时,水蒸发快 | 水分子受热,运动速率加快 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据分子的基本特征:分子质量和体积都很小;分子之间有间隔;分子是在不断运动的;同种的分子性质相同,不同种的分子性质不同,可以简记为:“两小运间,同同不不”,结合事实进行分析判断即可.
解答 解:A、水银是金属汞的俗称,是由汞原子直接构成的,用水银温度计测量体温,是因为汞原子间的间隔随着温度的改变而改变,故选项解释错误.
B、空气压缩可以变成液态空气,分子间有间隔,气体受压后,分子间隔变小,故选项解释正确.
C、冰水混合物属于纯净物,是因为都含有同种分子(水分子),故选项解释正确.
D、加热时,水蒸发快,是因为温度升高,水分子受热,运动速率加快,故选项解释正确.
故选:A.
点评 本题难度不大,掌握分子的基本性质(可以简记为:“两小运间,同同不不”)及利用分子的基本性质分析和解决问题的方法是解答此类题的关键.

练习册系列答案
相关题目
15.下列图象能正确反映相应操作过程的是( )
| A. | 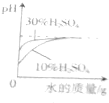 稀释等质量溶质质量分数分别为30%和10%的H2SO4溶液 | |
| B. | 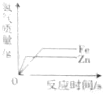 等质量的锌粉和铁粉,分别与质量分数相同的足量稀盐酸反应 | |
| C. |  在恒温条件下,将饱和的氯化钠溶液恒温蒸发水分至有白色晶体析出 | |
| D. | 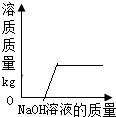 向氯化铜和硝酸铜的混合溶液中滴加氢氧化钠溶液 |
16.分析处理图表中的信息是学习化学的一种重要方法.
如表是KNO3、NaCl在不同温度下的溶解度(单位:g)
(1)20℃时,NaCl的溶解度是36g;
(2)30℃时,KNO3溶液的最大浓度(溶质质量分数)为$\frac{45.8g}{100g+45.8g}$×100%(只列计算式,不需要计算结果);
(3)KNO3中含少量氯化钠时,提纯硝酸钾的一般方法是冷却热饱和溶液;
(4)根据表内数据可知,KNO3和NaCl在某一温度时具有相同的溶解度X,则X的取值范围是36g~36.3g.
如表是KNO3、NaCl在不同温度下的溶解度(单位:g)
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| KNO3 | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | 246 |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
(2)30℃时,KNO3溶液的最大浓度(溶质质量分数)为$\frac{45.8g}{100g+45.8g}$×100%(只列计算式,不需要计算结果);
(3)KNO3中含少量氯化钠时,提纯硝酸钾的一般方法是冷却热饱和溶液;
(4)根据表内数据可知,KNO3和NaCl在某一温度时具有相同的溶解度X,则X的取值范围是36g~36.3g.
14.我国科学家屠呦呦因为“发现青蒿素(化学式为C15H22O5)-用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”而获诺贝尔奖,下列关于青蒿素的说法正确的是( )
| A. | 属于氧化物 | |
| B. | 由碳原子、氢原子和氧原子构成的 | |
| C. | 相对分子质量为282g | |
| D. | C、H、O三种元素的质量比为90:11:40 |
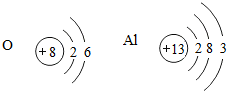 如图是氧和铝两种元素的原子结构示意图:
如图是氧和铝两种元素的原子结构示意图:
 近年开春一路飙升的菜价让市场大呼意外,“蒜你狠”也再次发威,某报社记者在山东金乡等大蒜主产区调查发现,产率下降、市场供求是这波“蒜你狠”行情的决定性因素.
近年开春一路飙升的菜价让市场大呼意外,“蒜你狠”也再次发威,某报社记者在山东金乡等大蒜主产区调查发现,产率下降、市场供求是这波“蒜你狠”行情的决定性因素.