题目内容
11. 要鉴别失去标签的稀硫酸和氢氧化钠溶液,小科、小妍各取适量的两种溶液于试管中,分别加入一定量经打磨的铝片,发现两支试管中均有气泡产生.
要鉴别失去标签的稀硫酸和氢氧化钠溶液,小科、小妍各取适量的两种溶液于试管中,分别加入一定量经打磨的铝片,发现两支试管中均有气泡产生.【提出问题】为什么两支试管中都会出现气泡呢?
【实验探究】请教老师后得知,氢氧化钠溶液也可以与铝发生反应产生气体.小科、小妍讨论后决定再一步验证:再取适量的两种溶液于试管中,分别滴入硫酸铜溶液,当观察到的现象是产生蓝色沉淀,该溶液是氢氧化钠溶液;没有明显现象的是稀硫酸.
【继续探究】铝和氢氧化钠溶液反应产生的气体是什么呢?
他们向老师要了相关的器材和药品进行了实验.
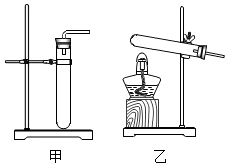
(1)用铝和氢氧化钠溶液制取这种气体,应该选用图甲.(选填“甲”或“乙”)
(2)收集该气体,经检验发现其具有可燃性,已知该气体是一种单质,则该气体为氢气.
分析 氢氧化钠和硫酸铜反应生成蓝色沉淀氢氧化铜和硫酸钠;
根据反应条件可以选择反应装置;
化学反应前后,元素种类不变,原子种类和总个数都不变.
解答 解:【实验探究】
再取适量的两种溶液于试管中,分别滴入硫酸铜溶液,当观察到产生蓝色沉淀时,该溶液是氢氧化钠溶液,没有明显现象的是稀硫酸.
故填:产生蓝色沉淀.
【继续探究】
(1)用铝和氢氧化钠溶液制取这种气体时不需要加热,应该选用图甲装置.
故填:甲.
(2)反应过程中,生成的气体可能是氢气、氧气等,氢气燃烧生成水,氧气不能燃烧,经检验发现其具有可燃性,并且该气体是一种单质,则该气体为氢气.
故填:氢气.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
6.下列物质的转化能实现的是( )
| A. | H2SO4$\stackrel{+BaCl_{2}}{→}$HCl | B. | CO $\stackrel{+NaOH}{→}$Na2CO3 | ||
| C. | Cu(OH)2 $\stackrel{+NaCl}{→}$NaOH | D. | NaNO3$\stackrel{+BaCO_{3}}{→}$ Ba(NO3)2 |
7.氯化钠是工业生产和生活的一种重要原料,也是实验室里常见的一种药品.如表是20℃时,氯化钠溶解于水的实验数据,回答下列问题;
(1)计算第1次实验得到的氯化钠溶液的溶质质量分数.
(2)m=13.6;
(3)在这4次实验中,得到的氯化钠溶液属于饱和溶液的是③④(填实验序号)
| 实验序号 | 水的质量(g) | 加入氯化钠的质量(g) | 溶液的质量(g) |
| ① | 10 | 2 | 12 |
| ② | 10 | 3 | 13 |
| ③ | 10 | 4 | 13.6 |
| ④ | 10 | 5 | m |
(2)m=13.6;
(3)在这4次实验中,得到的氯化钠溶液属于饱和溶液的是③④(填实验序号)
6.在一次化学实验中,同学们将饱和硫酸铜溶液逐滴加到5mL饱和氢氧化钠溶液中,观察到以下异常实验现象:
查阅资料可知:氢氧化铜在室温下稳定,70℃~80℃时分解生成氧化铜;氢氧化铜在氢氧化钠溶液中溶解生成铜酸钠[Na2Cu(OH)4],铜酸钠溶于水,溶液呈亮蓝色.
(1)硫酸铜溶液与氢氧化钠溶液生成蓝色沉淀的化学方程式为CuSO4+2NaOH=Na2SO4+Cu(OH)2↓.
(2)同学们推知饱和硫酸铜溶液与饱和氢氧化钠溶液的反应是放热反应,他们依据的实验现象是蓝色沉淀逐渐变为黑色.
(3)针对实验序号①中的异常现象,同学们进一步实验探究:
写出上述实验⑥中反应的化学方程式:2NaOH+Cu(OH)2=Na2Cu(OH)4.
| 实验序号 | 滴加CuSO4溶液的量 | 实验现象 |
| ① | 第1~6滴 | 产生蓝色沉淀,但振荡后沉淀消失,形成亮蓝色溶液 |
| ② | 第7~9滴 | 产生蓝色沉淀,且沉淀逐渐增多.振荡后沉淀不消失,很快沉淀逐渐变成黑色 |
(1)硫酸铜溶液与氢氧化钠溶液生成蓝色沉淀的化学方程式为CuSO4+2NaOH=Na2SO4+Cu(OH)2↓.
(2)同学们推知饱和硫酸铜溶液与饱和氢氧化钠溶液的反应是放热反应,他们依据的实验现象是蓝色沉淀逐渐变为黑色.
(3)针对实验序号①中的异常现象,同学们进一步实验探究:
| 实验序号 | 实验操作 | 实验现象 | 实验结论 |
| ③ | 向0.5g Cu(OH)2固体中加入5mL5%NaOH溶液,充分振荡 | 蓝色固体不消失 | 氢氧化铜能溶解在高于20%的氢氧化钠溶液中形成铜酸钠溶液 |
| ④ | 向0.5g Cu(OH)2固体中加入5mL10%NaOH溶液,充分振荡 | 蓝色固体不消失 | |
| ⑤ | 向0.5g Cu(OH)2固体中加入5mL20%NaOH溶液,充分振荡 | 蓝色固体减少 | |
| ⑥ | 向0.5g Cu(OH)2固体中加入5mL30%NaOH溶液,充分振荡 | 蓝色固体消失,得到亮蓝色溶液 |
16.对滤渣丙的分析正确的是( )
| A. | 若滤渣丙中有黑色固体,则滤渣丙中一定有铁 | |
| B. | 若滤液Ⅳ呈蓝色,则滤渣丙中一定有铁 | |
| C. | 若滤渣丙与固体丁的质量比大于4:5,则原固体由四种物质组成 | |
| D. | 若滤渣丙的质量小于固体丁的质量,则原固体由三种物质组成 |
20.我校自然科学兴趣小组在野外考察时带回来一矿石进行实验.请回答:
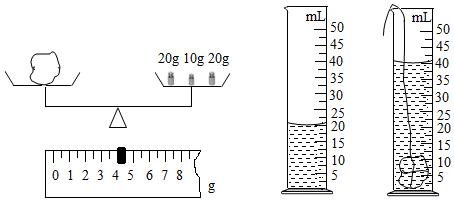
(1)下图是测定这块矿石的密度时所用的仪器及实验情况,计算出此矿石的密度.
(2)经检验此矿石中有一主要元素是钙元素,取此矿石(杂质不与盐酸反应,且不溶于水)8克放入烧杯中(烧杯的质量为20克),再加入47.2克稀盐酸,在一定时间内恰好反应,生成一种能使澄清石灰水变浑浊的气体.反应时间和烧杯及其所盛物质的总质量的关系如下表所示:
①生成气体的质量为2.2克;
②此矿石的主要成分是碳酸钙,求反应后所得溶液溶质的质量分数?
(1)下图是测定这块矿石的密度时所用的仪器及实验情况,计算出此矿石的密度.

(2)经检验此矿石中有一主要元素是钙元素,取此矿石(杂质不与盐酸反应,且不溶于水)8克放入烧杯中(烧杯的质量为20克),再加入47.2克稀盐酸,在一定时间内恰好反应,生成一种能使澄清石灰水变浑浊的气体.反应时间和烧杯及其所盛物质的总质量的关系如下表所示:
| 反应时间(秒) | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 20 |
| 烧杯及其所盛物质的总质量(克) | 75.2 | 74.8 | 74.4 | 74.0 | 73.6 | 73.2 | 73 | 73 | 73 | 73 |
②此矿石的主要成分是碳酸钙,求反应后所得溶液溶质的质量分数?