题目内容
4.化学的学科特征是在原子、分子基础上研究物质和创造物质.(1)从Na、Mg原子结构示意图(如图1)推知,钠原子质子数为11,金属Na、Mg化学性质不同的原因是最外层电子数不同;
(2)图2反应的化学方程式为2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;
(3)图3反应的实质是氢离子和氢氧根离子结合成水分子.
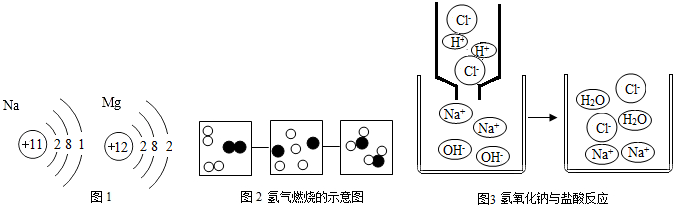
分析 (1)根据图1,获得质子数;在原子结构中,最外层的电子数决定元素的性质;物质的结构决定物质的性质;
(2)根据图2观察微粒的变化,书写化学方程式;
(3)根据图3观察微粒的变化,分析分子的形成.
解答 解:解:(1)从Na、Mg原子结构示意图推知,金属Na、Mg的最外层的电子数不同,决定了金属Na、Mg性质不同.
(2)由图1反应可知,氢气和氧气反应生成了水,反应的方程式是:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;
(3)由图3微粒的变化可知,图3反应的实质是氢离子和氢氧根离子结合成水分子.
故答案为:(1)11;最外层的电子数不同;(2)2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;(3)氢离子和氢氧根离子
点评 解答本题要充分理解图中提供的信息,只有这样才能确定物质的构成及种类,也才能正确的判断物质的化学式、反应的方程式.

练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目
15.自来水消毒过程中常会发生如下化学反应,其反应的微观过程可用如图表示,下列有关说法错误的是( )


| A. | 化学反应前后原子的种类和个数不改变 | |
| B. | 图乙表示的反应的基本反应类型是分解反应 | |
| C. | 化学反应的实质是分子破裂和原子的重新组合 | |
| D. | 图中C物质属于酸,D物质属于氧化物 |
19.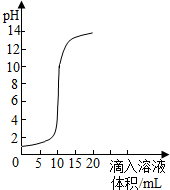 如图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.下列说法不正确的是( )
如图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.下列说法不正确的是( )
 如图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.下列说法不正确的是( )
如图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.下列说法不正确的是( )| A. | 该实验是将氢氧化钠溶液滴入盐酸中 | |
| B. | 氢氧化钠溶液和盐酸恰好反应时,溶液PH=7 | |
| C. | 当滴加入20ml溶液时,再滴加石蕊试剂,溶液呈红色 | |
| D. | 当pH=12时,所得溶液的溶质为NaCl和NaOH |
9. 根据图一、图二提供的信息进行判断,下列说法中,正确的是( )
根据图一、图二提供的信息进行判断,下列说法中,正确的是( )
 根据图一、图二提供的信息进行判断,下列说法中,正确的是( )
根据图一、图二提供的信息进行判断,下列说法中,正确的是( )| A. | 图一粒子容易形成阳离子 | |
| B. | 图二粒子属于非金属元素 | |
| C. | 图一和图二表示的元素容易反应形成化合物 | |
| D. | 图二粒子表示的元素在化合物中的化合价一般为-1价 |
13.现有15.6g CaO与CaCO3的固体混合物,测得其中钙元素与碳元素的质量比为20:3.在室温下,将该混合物与73g稀盐酸混合,恰好完全反应,所得不饱和溶液的质量为84.2g,则原固体混合物中含有钙元素的质量为下列的( )
| A. | 12g | B. | 8g | C. | 4.4g | D. | 4g |
14.下列实验操作中,正确的是( )
| A. |  倾倒液体 | B. |  取用固体粉末 | C. |  稀释浓硫酸 | D. |  熄灭酒精灯 |
 如图是二氧化碳的知识网络图(反应条件已略去).
如图是二氧化碳的知识网络图(反应条件已略去).