题目内容
13.现有15.6g CaO与CaCO3的固体混合物,测得其中钙元素与碳元素的质量比为20:3.在室温下,将该混合物与73g稀盐酸混合,恰好完全反应,所得不饱和溶液的质量为84.2g,则原固体混合物中含有钙元素的质量为下列的( )| A. | 12g | B. | 8g | C. | 4.4g | D. | 4g |
分析 根据质量守恒定律,反应前后总质量之差为二氧化碳的质量,根据二氧化碳的质量可求出碳元素的质量,根据钙元素与碳元素的质量比可求出钙元素的质量.
解答 解:根据质量守恒定律,反应前后总质量之差为二氧化碳的质量,为二氧化碳的质量为:15.6g+73g-84.2g=4.4g;
则碳元素的质量为:4.4g×$\frac{12}{44}×100%$=1.2g,钙元素与碳元素的质量比为20:3,则碳元素的质量为:1.2g×20÷3=8g.
故选B.
点评 根据质量守恒定律即可解答本题.

练习册系列答案
 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
3.下列实验操作中,正确的是( )
| A. | 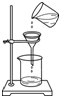 过滤 | B. | 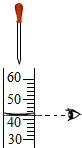 量取液体 | C. | 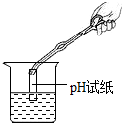 测定溶液的pH | D. | 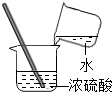 浓硫酸的稀释 |
8.下列叙述中,不正确的是( )
| A. | 过氧化氢分解反应是破坏旧分子、形成新分子的变化 | |
| B. | 复分解反应的实质是参加反应的物质间离子的互换 | |
| C. | 能使无色酚酞试液变红色的溶液一定是碱的溶液 | |
| D. | 化学变化的过程常会伴随能量变化 |
18.实验二中某学生的家长为即将参加中考的孩子设计了一份爱心晚餐:米饭、炒猪肝、清蒸鲫鱼.为均衡膳食,请补充一种食物使食谱营养更合理( )
| A. | 煎鸡蛋 | B. | 稀饭 | C. | 炒青菜 | D. | 五香牛肉 |
2. 溶解度可以表示物质溶解性的大小.
溶解度可以表示物质溶解性的大小.
①下表是KNO3在不同温度下的溶解度.
Ⅰ.40℃时,硝酸钾的溶解度为63.9g/100g水.
Ⅱ.40℃时将31g KNO3固体放入50g水中,所得溶液为不饱和溶液(填“饱和”或“不饱和”),若降温到20℃能析出固体15.2g.
Ⅲ.为测定x的值,取4份60℃的水各50g,分别进行实验,并记录数据如下表:
由实验可知CD
A.甲所得溶液中溶质质量分数为80%
B.乙恰好形成60℃时的饱和溶液
C.丙和丁所得溶液溶质质量分数相等
D.60℃时KNO3的溶解度为110g/100g水
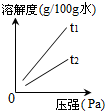
②气体的溶解度也有一定的变化规律.不同温度下,氧气的溶解度随压强变化如图所示,图中t1对应的温度为40℃,则t2对应的温度C
A.小于40℃B.等于40℃C.大于40℃D.无法确定.
 溶解度可以表示物质溶解性的大小.
溶解度可以表示物质溶解性的大小.①下表是KNO3在不同温度下的溶解度.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度(g/100g水) | 13.3 | 31.6 | 63.9 | x | 169 | 246 |
Ⅱ.40℃时将31g KNO3固体放入50g水中,所得溶液为不饱和溶液(填“饱和”或“不饱和”),若降温到20℃能析出固体15.2g.
Ⅲ.为测定x的值,取4份60℃的水各50g,分别进行实验,并记录数据如下表:
| 实验编号 | 甲 | 乙 | 丙 | 丁 |
| KNO3质量/g | 40 | 50 | 60 | 70 |
| H2O质量/g | 50 | 50 | 50 | 50 |
| 溶液质量/g | 90 | 100 | 105 | 105 |
A.甲所得溶液中溶质质量分数为80%
B.乙恰好形成60℃时的饱和溶液
C.丙和丁所得溶液溶质质量分数相等
D.60℃时KNO3的溶解度为110g/100g水
②气体的溶解度也有一定的变化规律.不同温度下,氧气的溶解度随压强变化如图所示,图中t1对应的温度为40℃,则t2对应的温度C
A.小于40℃B.等于40℃C.大于40℃D.无法确定.