题目内容
9. 自从央行公告第四套人名币1角硬币从2016年11月1日起只收不付后,“菊花1角”身价飞涨.一个很重要的原因是,“菊花1角”材质特殊导致日渐稀少,其使用了铝锌材质.铝、锌元素的部分信息如下,则说法正确的是( )
自从央行公告第四套人名币1角硬币从2016年11月1日起只收不付后,“菊花1角”身价飞涨.一个很重要的原因是,“菊花1角”材质特殊导致日渐稀少,其使用了铝锌材质.铝、锌元素的部分信息如下,则说法正确的是( )| A. | 铝比锌的金属活泼性更弱 | |
| B. | 相等质量的铝和锌和足量稀硫酸反应,铝产生的氢气多 | |
| C. | 锌原子的最外层电子数比铝多17 | |
| D. | 铝的相对原子质量为26.98% |
分析 A、根据金属活动性顺序表分析判断;
B、根据金属与酸的反应分析判断;
C、根据核外电子排布的规律分析判断;
D、根据元素周期表中一个格的含义分析判断.
解答 解:A、铝比锌的金属活泼性更强,故A错误;
B、由产生氢气的质量=$\frac{金属的化合价}{金属的相对原子质量}×金属的质量$可知,相等质量的铝和锌和足量稀硫酸反应,铝产生的氢气多,故B正确;
C、由于最外层电子数不超过8个,锌原子的核外电子数比铝多17,不是最外层电子数比铝多17,故C错误;
D、由元素周期表中一个格的含义可知,铝的相对原子质量为26.98,单位是“1”,故D错误.
故选B.
点评 本题难度不大,考查学生灵活运用元素周期表中元素的信息进行分析解题的能力,了解元素周期表中一个格的含义是解答本题的基础知识.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
19.某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示)的无色溶液,他们对此产生了兴趣.
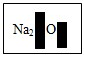
【提出问题】这瓶溶液究竟是什么?
经过询问实验老师得知,这瓶物色溶液应该是碳酸钠、碳酸氢钠、氧化钠、硫酸钠、硝酸钠中的一种.为了确定该药品,他们首先根据标签上残留的信息进行如下分析:
(1)小明认为组成中含有氧元素,该溶液一定不是NaCl氯化钠溶液.
(2)小英提出,碳酸氢钠、硝酸钠也不可能,你认为她的依据是这二者的化学式中Na元素的右下角不会是2.
为了确定该溶液究竟是剩余两种盐的哪一种,他们设计了如下实验:
【设计实验】
【实验结论】
(3)这瓶无色溶液是Na2CO3.生成白色沉淀过程的化学方程式是BaCl2+Na2CO3═BaCO3↓+2NaCl.
【实验反思】
(4)小强认为上述设计实验还可简化,仍能达到目的.小强的实验操作是取少量无色溶液样品于试管中,慢慢滴加稀盐酸,看是否产生气泡少量无色溶液样品于试管中,慢慢滴加稀盐酸,看是否产生气泡.经查阅资料得知上述五种盐里碳酸钠、碳酸氢钠的溶液呈碱性,其余三种盐的溶液呈中性,请你再设计一种实验方法,确定该溶液究竟是哪种盐.简述实验操作和现象在玻璃片上放一小片pH试纸,将样品液滴到试纸上,把试纸显示的颜色与标准比色卡比较,测得溶液pH大于7.(或取少量无色溶液样品于试管中,滴加几滴无色酚酞,观察到溶液变红等.).

【提出问题】这瓶溶液究竟是什么?
经过询问实验老师得知,这瓶物色溶液应该是碳酸钠、碳酸氢钠、氧化钠、硫酸钠、硝酸钠中的一种.为了确定该药品,他们首先根据标签上残留的信息进行如下分析:
(1)小明认为组成中含有氧元素,该溶液一定不是NaCl氯化钠溶液.
(2)小英提出,碳酸氢钠、硝酸钠也不可能,你认为她的依据是这二者的化学式中Na元素的右下角不会是2.
为了确定该溶液究竟是剩余两种盐的哪一种,他们设计了如下实验:
【设计实验】
| 实验操作 | 实验现象 |
| 取少量样品于试管中,慢慢滴加BaCl2溶液,静置一段时间,倾去上层清液,向沉淀中继续滴加稀盐酸 | 先出现白色沉淀,后产生大量气泡 |
(3)这瓶无色溶液是Na2CO3.生成白色沉淀过程的化学方程式是BaCl2+Na2CO3═BaCO3↓+2NaCl.
【实验反思】
(4)小强认为上述设计实验还可简化,仍能达到目的.小强的实验操作是取少量无色溶液样品于试管中,慢慢滴加稀盐酸,看是否产生气泡少量无色溶液样品于试管中,慢慢滴加稀盐酸,看是否产生气泡.经查阅资料得知上述五种盐里碳酸钠、碳酸氢钠的溶液呈碱性,其余三种盐的溶液呈中性,请你再设计一种实验方法,确定该溶液究竟是哪种盐.简述实验操作和现象在玻璃片上放一小片pH试纸,将样品液滴到试纸上,把试纸显示的颜色与标准比色卡比较,测得溶液pH大于7.(或取少量无色溶液样品于试管中,滴加几滴无色酚酞,观察到溶液变红等.).
20.有关实验现象的描述正确的是( )
| A. | 硫在空气中燃烧发出明亮的蓝紫色火焰 | |
| B. | 铁丝在氧气中剧烈燃烧,火星四射 | |
| C. | 干冰在空气中升华,周围出现白色烟雾 | |
| D. | 碳在空气中剧烈燃烧,发出白光 |
4.对于化学反应A+B═C+D,下列说法错误的是( )
| A. | 若A、C为单质,B、D为化合物,则该反应一定是置换反应 | |
| B. | 若C、D分别为盐和水,则该反应一定是中和反应 | |
| C. | 若A、B为化合物,则该反应可能是复分解反应 | |
| D. | 无论A、B、C、D为哪类物质,该反应不可能是化合反应和分解反应 |
14.阿司匹林的化学式为C9H8O4,有关说法正确的是( )
| A. | 其相对原子质量是180g | |
| B. | 该分子中有三种元素 | |
| C. | 该物质中氢元素质量分数最大 | |
| D. | 该物质中碳、氢、氧原子个数比为9:8:4 |
1.百合中的秋水仙碱具有润肺止咳功效,其化学式为C22H25NO6.下列说法正确的是( )
| A. | 秋水仙碱中氧元素的质量分数约为24% | |
| B. | 秋水仙碱中碳、氢元素质量比为22:25 | |
| C. | 秋水仙碱由22个碳原子、25个氢原子、1个氮原子、6个氧原子构成 | |
| D. | 秋水仙碱中氢元素的质量分数最大 |
18.实验室有98.5g碳酸钡样品(杂质既不溶于水,也不与酸反应),与100g氢元素质量分数为10%的稀硫酸恰好完全反应,则样品中碳酸钡的质量分数为( )
| A. | 25% | B. | 12.5% | C. | 19.7% | D. | 20% |
19.化学与生活密切相关,下列叙述正确的是( )
| A. | 人体体液的pH必须维持在一定范围内,pH过小会造成“酸中毒” | |
| B. | 人体缺钙会引起骨质疏松症,因此钙元素摄入得越多越好 | |
| C. | 食品添加剂对人体健康都有害,应禁止其使用 | |
| D. | 铵态氮肥与草木灰混合施用可以明显提高肥效 |