题目内容
某化学兴趣小组在实验室做了如图所示的A、B两个实验.
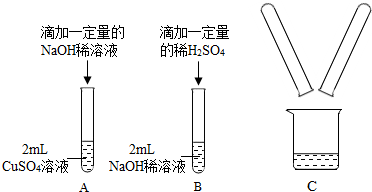
(1)A实验中发生反应的化学方程式为 .
(2)A、B两个实验结束后,小组同学将两支试管中的物质同时倒入一洁净的烧杯中(如图所示),混合后,观察到烧杯中有蓝色沉淀.同学们将烧杯内的物质过滤,对所得滤液中溶质的成分进行探究.
【猜想】小明猜想:滤液中的溶质是Na2SO4、CuSO4;
小光猜想:滤液中的溶质是Na2SO4、NaOH;
小英猜想:滤液中的溶质是Na2SO4、CuSO4、H2SO4;
你的猜想:滤液中的溶质还可能是 .
【讨论】你认为 的猜想一定不合理.理由是 .
如果滤液为无色,还可排除 的猜想,理由是 .
【实验】若小光的猜想正确,请完成下表的方案.

(1)A实验中发生反应的化学方程式为
(2)A、B两个实验结束后,小组同学将两支试管中的物质同时倒入一洁净的烧杯中(如图所示),混合后,观察到烧杯中有蓝色沉淀.同学们将烧杯内的物质过滤,对所得滤液中溶质的成分进行探究.
【猜想】小明猜想:滤液中的溶质是Na2SO4、CuSO4;
小光猜想:滤液中的溶质是Na2SO4、NaOH;
小英猜想:滤液中的溶质是Na2SO4、CuSO4、H2SO4;
你的猜想:滤液中的溶质还可能是
【讨论】你认为
如果滤液为无色,还可排除
【实验】若小光的猜想正确,请完成下表的方案.
| 实验步骤 | 预期的实验现象 | 实验结论 |
| 取少量滤液于试管中,滴入 | 小光的猜想正确 |
考点:碱的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的碱 碱的通性
分析:根据已有的知识进行分析,氢氧化钠能与硫酸反应生成硫酸钠和水;硫酸铜能与氢氧化钠反应生成氢氧化铜沉淀,氢氧化铜能与硫酸反应生成硫酸铜和水;酚酞试液在碱性溶液中为红色,据此解答.
解答:解:
(1)A实验中氢氧化钠与硫酸铜溶液反应,故发生反应的化学方程式为2NaOH+CuSO4=Cu(OH)2↓+Na2SO4;
(2)硫酸铜能与氢氧化钠反应生成氢氧化铜沉淀和硫酸钠,氢氧化钠能与硫酸反应生成硫酸钠,故滤液中一定含有硫酸钠,故填:Na2SO4;
由于烧杯中含有蓝色沉淀氢氧化铜,而氢氧化铜能与硫酸反应生成易溶于水的硫酸铜,故一定不会含有硫酸,所以小英的猜想一定不正确;硫酸铜溶液是蓝色的,若滤液是无色的,则小明的猜想不正确,故填:小英,小明,滤液中含有硫酸铜,溶液呈蓝色;
小光的猜想中,含有氢氧化钠,氢氧化钠的水溶液呈碱性,能使酚酞试液变红,故可以使用酚酞试液来证明,故填:
故答案为:
(1)2NaOH+CuSO4=Cu(OH)2↓+Na2SO4;
【猜想】你的猜想:Na2SO4(或硫酸钠);
【讨论】小英、Cu(OH)2沉淀和H2SO4不能共存,烧杯中既然有Cu(OH)2沉淀,那滤液中的溶质就没有H2SO4了(两空全对得,答对一个不得分). 小明、溶液中含有硫酸铜,溶液显蓝色(两空全对得,答对一个不得分).
【实验】酚酞试液等指示剂( CuSO4等可溶性盐溶液 )、溶液由无色变为红色(有蓝色沉淀生成等生成有颜色的沉淀)(其他答案只要合理也得分)
(1)A实验中氢氧化钠与硫酸铜溶液反应,故发生反应的化学方程式为2NaOH+CuSO4=Cu(OH)2↓+Na2SO4;
(2)硫酸铜能与氢氧化钠反应生成氢氧化铜沉淀和硫酸钠,氢氧化钠能与硫酸反应生成硫酸钠,故滤液中一定含有硫酸钠,故填:Na2SO4;
由于烧杯中含有蓝色沉淀氢氧化铜,而氢氧化铜能与硫酸反应生成易溶于水的硫酸铜,故一定不会含有硫酸,所以小英的猜想一定不正确;硫酸铜溶液是蓝色的,若滤液是无色的,则小明的猜想不正确,故填:小英,小明,滤液中含有硫酸铜,溶液呈蓝色;
小光的猜想中,含有氢氧化钠,氢氧化钠的水溶液呈碱性,能使酚酞试液变红,故可以使用酚酞试液来证明,故填:
| 实验步骤 | 预期的实验现象 | 实验结论 |
| 取少量滤液于试管中,滴入 酚酞试液等指示剂( CuSO4等可溶性盐溶液 )、 | 溶液由无色变为红色(有蓝色沉淀生成等生成有颜色的沉淀) | 小光的猜想正确 |
(1)2NaOH+CuSO4=Cu(OH)2↓+Na2SO4;
【猜想】你的猜想:Na2SO4(或硫酸钠);
【讨论】小英、Cu(OH)2沉淀和H2SO4不能共存,烧杯中既然有Cu(OH)2沉淀,那滤液中的溶质就没有H2SO4了(两空全对得,答对一个不得分). 小明、溶液中含有硫酸铜,溶液显蓝色(两空全对得,答对一个不得分).
【实验】酚酞试液等指示剂( CuSO4等可溶性盐溶液 )、溶液由无色变为红色(有蓝色沉淀生成等生成有颜色的沉淀)(其他答案只要合理也得分)
点评:本题考查了常见的物质的性质,完成此题,可以依据已有的知识进行.要求同学们加强对基础知识的储备,以便灵活应用.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案
相关题目
某物质的充分燃烧产物是CO2和H2O,为了确定该物质的元素组成,某小组设计了如图所示实验(其中浓硫酸、无水CaCl2均为常用干燥剂,部分固定装置省略).称取0.84g待测物完全燃烧后,称得D装置增重1.08g,E装置增重2.64g.则下列推断正确的是( )


| A、该物质一定含有C、H元素,没有氧元素 |
| B、该物质一定含有C、H、O元素 |
| C、用充有空气的储气球代替装置A、B更有利于实验的进行 |
| D、氧化铜的有无对实验结果没有影响 |
 如表所列各组物质中,物质之间按箭头方向通过一步反应就能实现如图所示转化的是( )
如表所列各组物质中,物质之间按箭头方向通过一步反应就能实现如图所示转化的是( )

 图中表示的是几种常见物质的转化关系(部分反应物、生成物及反应条件省略),已知C为生活中不可缺少的调味品,F为某种建筑材料的主要成分,请回答以下问题:
图中表示的是几种常见物质的转化关系(部分反应物、生成物及反应条件省略),已知C为生活中不可缺少的调味品,F为某种建筑材料的主要成分,请回答以下问题:

