题目内容
实验小组设计了分离NaCl和CaCl2两种固体的实验方案,据此回答问题:
(1)写出试剂X的化学式 ;
(2)加入过量X溶液,过滤后所得滤液中含有的溶质是 (化学式),在滤液中加入适量Y后,蒸发即可得到较纯净的NaCl固体,写出有关的化学方程式 .

(1)写出试剂X的化学式
(2)加入过量X溶液,过滤后所得滤液中含有的溶质是
考点:混合物的分离方法,酸的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:物质的分离和提纯
分析:(1)分离NaCl和CaCl2两种固体混合物,溶解后加入过量碳酸钠溶液,生成碳酸钙沉淀和氯化钠,碳酸钙和盐酸反应得到氯化钙溶液,经蒸发可得到氯化钙固体;
(2)由于碳酸钠过量,所以滤液中的物质有氯化钠和碳酸钠,因此要得到纯净的氯化钠就需要除去碳酸钠,加入稀盐酸最合适,碳酸钠和稀盐酸生成氯化钠和水和二氧化碳,蒸发后最后的固体物质是氯化钠.
(2)由于碳酸钠过量,所以滤液中的物质有氯化钠和碳酸钠,因此要得到纯净的氯化钠就需要除去碳酸钠,加入稀盐酸最合适,碳酸钠和稀盐酸生成氯化钠和水和二氧化碳,蒸发后最后的固体物质是氯化钠.
解答:解:(1)NaCl和CaCl2两种固体混合物,溶解后加入过量碳酸钠溶液,生成碳酸钙沉淀和氯化钠,过滤后得到的沉淀B为碳酸钙,碳酸钙和盐酸反应生成氯化钙溶液,经蒸发可得到氯化钙固体,所以试剂X为碳酸钠溶液;故填:Na2CO3;
(2)由于碳酸钠过量,所以滤液中的物质有氯化钠和碳酸钠,因此要得到纯净的氯化钠就需要除去碳酸钠,向滤液中加入适量盐酸至不产生气体,生成氯化钠和水和二氧化碳,蒸发后最后的固体物质是氯化钠,化学方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑.
故答案为:NaCl、Na2CO3;Na2CO3+2HCl=2NaCl+H2O+CO2↑.
(2)由于碳酸钠过量,所以滤液中的物质有氯化钠和碳酸钠,因此要得到纯净的氯化钠就需要除去碳酸钠,向滤液中加入适量盐酸至不产生气体,生成氯化钠和水和二氧化碳,蒸发后最后的固体物质是氯化钠,化学方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑.
故答案为:NaCl、Na2CO3;Na2CO3+2HCl=2NaCl+H2O+CO2↑.
点评:本题是一道考查固固混合物分离的方法,除杂题是初中化学常见题型,它灵活多变,可以综合考查学生的解题能力.混合物分离或提纯方法综合可以分为两大类:一类是物理方法(如过滤和结晶等),一类是化学方法(如沉淀法,气体法,置换法和吸收法等).

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
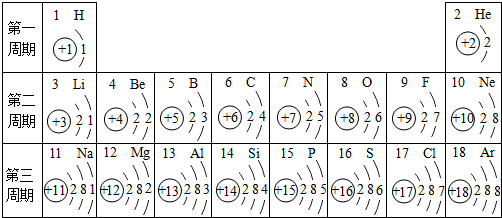
下列元素属于金属的是( )
| A、C | B、N | C、S | D、Ag |