题目内容
10.如图是五种粒子的结构示意图: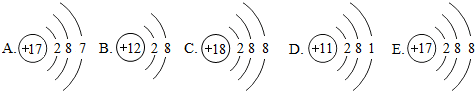
(1)图中粒子共能表示4种元素.A所表示的元素位于元素周期表的第3周期.
(2)图中表示的阳离子是Mg2+(用离子符号表示),表示的阴离子是Cl-(用离子符号表示),二者形成的化合物的化学式为MgCl2.
分析 同种元素形成的粒子,质子数相同,原子呈电中性,对阳离子而言,核电荷数>核外电子数.如何找出原子和离子的区别,可以从质子数与核外电子的关系、粒子的带电性等方面加以考虑.原子的核外电子层数表示该元素所处的周期.
解答 解:(1)A与E核内质子数相同,表示同一种元素,所以共有4种元素.A原子核外有3个电子层,所以其表示的元素在第3周期.所以答案为:4;3.
(2)A、C和D中,核电荷数=核外电子数,表示原子,B中核电荷数>核外电子数,失去2个电子,表示阳离子,形成化合物时常显示+2价,质子数为12,所以该粒子表示镁离子,E中核电荷数<核外电子数,得到1个电子,表示阴离子,形成化合物时常显示-1价,质子数为17,所以该粒子表示氯离子,它们形成的化合物为氯化镁.所以答案为:Mg2+;Cl-;MgCl2.
答案:(1)4;3;
(2)Mg2+;Cl-;MgCl2.
点评 本题注重基础,考查知识点较多,并且题目难度不很大,对基础知识的掌握有很大帮助,多注重一些规律的记忆和积累.

练习册系列答案
相关题目
13.如图是某空间站能量转化系统局部示意图,其中水电解系统及燃料电池系统中的溶液均采用氢氧化钠溶液.下列有关说法错误的是( )


| A. | 该能量转化系统中的水可以循环使用 | |
| B. | 水电解系统中负极产生的气体能使带火星的木条复燃 | |
| C. | 燃料电池系统产生的能量实际上来自于水 | |
| D. | 水电解系统中加入氢氧化钠溶液,目的是为了增强水的导电性 |
1.在空气中氧气含量的探究实验中,你认为适用的物质是( )
| A. | 石蜡 | B. | 红磷 | C. | 白磷 | D. | 铁丝 |
15.取一定质量的CaCO3高温加热一段时间后,冷却,测得剩余固体的质量为8.0g,剩余固体中钙元素质量分数为50.0%.下列判断正确的是( )
| A. | 生成2.0 gCO2气体 | B. | 原来CaCO3的质量为14.3 g | ||
| C. | 生成了5.6 gCaO | D. | 剩余CaCO3的质量为3.0 g |
2.现将Fe2O3、CuO、Al2O3的混合物16克,与109.5克20%的稀盐酸混合后恰好完全反应,则此金属氧化物金属元素的含量是( )
| A. | 70% | B. | 20% | C. | 73.5% | D. | 80% |
19.家庭厨房使用的口碱主要成分是一种含钠的化合物,将盐酸加入口碱时,放出一种无色、无气味、能使澄清石灰水变浑浊的气体,由此推知这种化合物是下列四种物质中的( )
| A. | NaCl | B. | Na2CO3 | C. | NaOH | D. | NaClO3 |

 甲、乙、丙是三个实验的示意图,根据图中所发生的化学反应现象及化学反应原理,进行总结归纳并回答下列问题:
甲、乙、丙是三个实验的示意图,根据图中所发生的化学反应现象及化学反应原理,进行总结归纳并回答下列问题: