题目内容
6.高铁酸钠(Na2FeO4)是一种“绿色”环保的高效净水剂,制得高铁酸钠的化学反应方程式为:2Fe(NO3)3+3X+10NaOH═2Na2FeO4+3NaCl+6NaNO3+5H2O.下列说法中正确的是( )| A. | X的化学式为NaClO3 | |
| B. | 高铁酸钠中铁元素质量分数最大 | |
| C. | 生成物中有三种盐和一种氧化物 | |
| D. | 该反应中,只有铁元素的化合价发生了变化 |
分析 A、根据质量守恒定律的实质,反应前后各元素的原子个数相等推断X的化学式;
B、根据元素质量比中最大的元素的质量分数最大进行解答;
C、根据盐和氧化物的定义进行解答;
D、根据化合价求解分析.
解答 解:A、因为反应前后各元素原子个数相等,反应前:Fe原子2个,N原子6个,Na原子10个,O原子28个,H原子10个;反应后:Fe原子2个,N原子6个,Na原子13个,O原子31个,H原子10个,Cl原子3个;X的化学式为NaClO,故说法错误;
B、高铁酸钠中各种元素的质量比为:Fe:Na:O=56×2:23×6:16×9=56:69:72,故氧元素的质量分数最大,故说法错误
C、Na2FeO4、3NaCl、NaNO3属于盐;H2O是氧化物,故说法正确;
D、反应中Cl的化合价由+1价到-1价,故D说法错误;
故选:C.
点评 本题考查化合价原则、盐和氧化物定义以及质量守恒定律的内容等,考查注重基础.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.生活中许多变化都能产生热量,下列放热现象主要由物理变化引起的是( )
| A. | 天然气燃烧放热 | B. | 白炽灯泡通电放热 | ||
| C. | 生石灰与水混合放热 | D. | 苹果腐烂发热 |
14.化学与人类生活衣食住行紧密相关.
(1)下列服装材料不属于天然材料制成的是B.(填标号)
A.100%羊毛衫 B.涤纶连衣裙 C.真丝旗袍 D.纯棉T恤
(2)自热米饭是一中快餐食品.请根据下图及表信息,回答下列问题:

①图2包装材料一般是符合卫生标准的铝箔.铝可以压制成铝箔,说明铝具有良好的延展性.
②该自热米饭是利用发热包中的生石灰与水反应放出热量来进行加热,生石灰与水反应的化学方程式为CaO+H2O═Ca(OH)2.
(3)良好的家居环境带来美好的生活.
①房屋装修后,可在室内放一些活性炭来吸收装修材料释放出的甲醛、苯等有毒气体,这是利用活性炭的吸附性.
②图3所示的“火立熄”是一种新型的家用灭火用品.“火立熄”接触到火焰3-5秒后炸开,释放的粉末覆盖在燃烧物上,同时放出不可燃烧气体,使火焰熄灭.“火立熄”的灭火原理是使燃烧物与氧气隔绝.(填标号)
A.清除可燃物 B.使燃烧物与氧气隔绝 C.降低燃烧物的着火点
(4)汽车是现代生活中常见的一种交通工具.
①喷漆可以延缓汽车钢铁外壳的锈蚀,起防锈原理是隔绝水和氧气.高炉炼铁的化学反应原理(冶炼赤铁矿化学方程式)3CO+Fe203$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
②汽车的燃料主要是汽油,汽油的成分复杂,本题用C8H18代表.
㈠C8H18完全燃烧的化学方程式为2C8H18+25O2 $\frac{\underline{\;点燃\;}}{\;}$16CO2+18H2O.
㈡公共汽车和出租车的耗油量近似值(均以汽油为燃料)和载客量(含驾驶员)如下表:
乘出租车行驶相同距离,人均耗油即排放二氧化碳是乘公共汽车的5倍.所以科技在进步,但出行还是乘坐公共汽车最环保.
(1)下列服装材料不属于天然材料制成的是B.(填标号)
A.100%羊毛衫 B.涤纶连衣裙 C.真丝旗袍 D.纯棉T恤
(2)自热米饭是一中快餐食品.请根据下图及表信息,回答下列问题:

| 营养素 | 每份含量 |
| 蛋白质 | 29.6g |
| 油脂 | 23.5g |
| 糖类 | 104.7g |
| 钠 | 814mg |
| 钙 | 130mg |
②该自热米饭是利用发热包中的生石灰与水反应放出热量来进行加热,生石灰与水反应的化学方程式为CaO+H2O═Ca(OH)2.
(3)良好的家居环境带来美好的生活.
①房屋装修后,可在室内放一些活性炭来吸收装修材料释放出的甲醛、苯等有毒气体,这是利用活性炭的吸附性.
②图3所示的“火立熄”是一种新型的家用灭火用品.“火立熄”接触到火焰3-5秒后炸开,释放的粉末覆盖在燃烧物上,同时放出不可燃烧气体,使火焰熄灭.“火立熄”的灭火原理是使燃烧物与氧气隔绝.(填标号)
A.清除可燃物 B.使燃烧物与氧气隔绝 C.降低燃烧物的着火点
(4)汽车是现代生活中常见的一种交通工具.
①喷漆可以延缓汽车钢铁外壳的锈蚀,起防锈原理是隔绝水和氧气.高炉炼铁的化学反应原理(冶炼赤铁矿化学方程式)3CO+Fe203$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
②汽车的燃料主要是汽油,汽油的成分复杂,本题用C8H18代表.
㈠C8H18完全燃烧的化学方程式为2C8H18+25O2 $\frac{\underline{\;点燃\;}}{\;}$16CO2+18H2O.
㈡公共汽车和出租车的耗油量近似值(均以汽油为燃料)和载客量(含驾驶员)如下表:
| 公共汽车 | 出租车 | |
| 百公里耗油/kg | 18 | 9 |
| 平均载客量/人 | 30 | 3 |
18.下列选项中物质的俗名和化学名称表示同一物质的是( )
| A. | 纯碱 氢氧化钠 | B. | 干冰 水 | ||
| C. | 生石灰 碳酸钙 | D. | 小苏打 碳酸氢钠 |
15.氢化钙固体是登山运动员常用的能源提供剂.某探究小组的同学通过查阅资料得知,氢化钙(CaH2)遇水反应生成氢氧化钙和氢气,请写出该反应的化学方程式CaH2+2H2O═Ca(OH)2+2H2↑.
探究小组的同学把一定量的CaH2加入Na2CO3溶液中,充分反应后过滤,得到滤渣和滤液.经检验滤渣的成份是碳酸钙.
【提出问题】滤液中溶质的成份是什么?
【猜想与假设】
猜想一:NaOH
猜想二:NaOH和Ca(OH)2
猜想三:NaOH和Na2CO3
猜想四:NaOH、Na2CO3和Ca(OH)2
经过讨论,大家认为猜想四不合理,用化学方程式说明原因Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
【实验证明】
【反思与拓展】
(1)向CaH2和足量水反应后的溶液加入NH4Cl溶液,产生的气体是氧气、氨气.
(2)登山运动员常用CaH2作为能源提供剂,与氢气相比,其优点是携带安全.
探究小组的同学把一定量的CaH2加入Na2CO3溶液中,充分反应后过滤,得到滤渣和滤液.经检验滤渣的成份是碳酸钙.
【提出问题】滤液中溶质的成份是什么?
【猜想与假设】
猜想一:NaOH
猜想二:NaOH和Ca(OH)2
猜想三:NaOH和Na2CO3
猜想四:NaOH、Na2CO3和Ca(OH)2
经过讨论,大家认为猜想四不合理,用化学方程式说明原因Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
【实验证明】
| 实验 | 现象 | 结论 |
| 实验一:取滤液,向其中滴入少量碳酸钠溶液 | Ⅰ:没有产生沉淀 | 猜想二不成立 |
| 实验二:另取滤液,向其中加入足量稀盐酸 | Ⅱ:产生气泡 | 猜想三成立 |
(1)向CaH2和足量水反应后的溶液加入NH4Cl溶液,产生的气体是氧气、氨气.
(2)登山运动员常用CaH2作为能源提供剂,与氢气相比,其优点是携带安全.


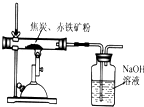 为了测定某赤铁矿中氧化铁(Fe2O3)的质量分数,化学兴趣小组的同学设计了两种实验方案(假设该赤铁矿中的杂质既不溶于水,也不发生反应).
为了测定某赤铁矿中氧化铁(Fe2O3)的质量分数,化学兴趣小组的同学设计了两种实验方案(假设该赤铁矿中的杂质既不溶于水,也不发生反应).