题目内容
6.某同学配制50g溶质质量分数为5%的KCl溶液,准备了下列实验用品.回答下列问题:
(1)该同学按下列实验步骤进行:$①\\;\\;\\;计算$计算,②称量,③量取,④溶解(填步骤名称)⑤装瓶.
(2)配制过程还缺少的一种玻璃仪器是玻璃棒(填名称).
(3)为了达到本实验目的,应用量筒量取47.5mL的水倒入烧杯中.
(4)已知氯化钾20℃时的溶解度是34g,50℃时溶解度是42,6g,通过如图所示的实验操作得到相应的溶液,在所得溶液中,属于不饱和溶液的是①③(填字母,下同),溶质的质量分数相同的是②⑤.

分析 (1)根据配制溶液的步骤解答;
(2)根据配置溶液所需仪器解答;
(3)根据溶质质量=溶液质量×溶质质量分数解答;
(4)根据固体的溶解度是指在一定温度下,某固体物质在100g水中达到饱和状态时所溶解的质量,根据固体物质的溶解度可以判断出在一定温度时形成的溶液是否饱和进行解答.
解答 解:
(1)配制溶液的步骤是::①计算,②称量,③量取,④溶解;
(2)配制过程除了用到图中所需仪器,还缺少玻璃棒;
(3)配制50g溶质质量分数为5%的KCl溶液,需KCl的质量为0g×5%=2.5g;水的质量=50g-2.5g=47.5g,合47.5mL;
(4)由于氯化钾在20℃时的溶解度是34g,即100g水中最多溶解34g氯化钾,因此在20℃时在100g水中加入20g氯化钾,氯化钾会全部溶解,得到的①溶液是20℃不饱和溶液;又加入20g氯化钾,由于在100g水中最多溶解34g氯化钾,因此这20g氯化钾只能再溶解14g,所以形成的②溶液是20℃饱和溶液;升温至50℃,由于氯化钾在50℃时的溶解度是42.6g,因此后加入的氯化钾会全部溶解,而且形成的溶液③是50℃不饱和溶液,但又加入20g氯化钾,这20g氯化钾会再溶解2.6g,形成的溶液④是50℃饱和溶液,然后降温到20℃时,有晶体析出,形成溶液⑤是20℃饱和溶液.
答案:(1)溶解;(2)玻璃棒; (3)47.5;(4)①③②⑤.
点评 本题难度不大,主要考查了对固体溶解度概念的理解,从而培养学生对知识的应用能力和理解能力.熟练掌握配制溶液的步骤,仪器,溶质的质量分数计算是解答此题的基础和关键.

练习册系列答案
 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
14.某工厂排放废水中含有AgNO3和Cu(NO3)2,为防止水体污染,现往废水中加入一定量的铁粉,充分反应后,过滤,往滤液中滴几滴稀盐酸,有白色沉淀生成,则下列说法正确的是( )
| A. | 滤液中一定含有硝酸亚铁和硝酸银,可能含有硝酸铜 | |
| B. | 滤液中一定含有硝酸亚铁、硝酸银、硝酸铜 | |
| C. | 滤渣中一定含有铁、银、铜 | |
| D. | 滤渣中一定含有银,可能含有铜 |
1.如图是某化学反应的微观示意图,其中“○”和“●”表示不同的元素的原子,下列有关说法正确的是( )


| A. | 该反应为置换反应 | |
| B. | 参加反应的“ ”和“ ”和“ ”分子个数比是3:1 ”分子个数比是3:1 | |
| C. | 反应前后分子和原子的总数目不变 | |
| D. | 反应物和生成物中共含有三种元素 |
11.表列出了除去物质中所含少量杂质的方法,其中正确的选项是正确的是( )
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | 铝粉 | 铁粉 | 加入过量稀盐酸,过滤 |
| B | 二氧化碳 | 一氧化碳 | 通入氧气,点燃 |
| C | 氯化钾 | 氯酸钾 | 加热 |
| D | 氢氧化钠溶液 | 碳酸钠 | 加入适量的稀盐酸 |
| A. | A | B. | B | C. | C | D. | D |
16.碳在空气中燃烧可以生成CO或CO2.那么,氢气中空气中燃烧除生成水以外,能不能生成其他产物?某研究小组进行了如下探究:
【提出猜想】氢气在空气中燃烧可能生成过氧化氢
【查阅资料】①过氧化氢能使紫色酸性KMnO4溶液褪色;②锌粒与稀H2SO4反应制取氢气可能混有使酸性高锰酸钾溶液褪色的物质.
【设计并完成实验】小明设计了下图所示三套实验装置,点燃氢气并收集液体燃烧物.
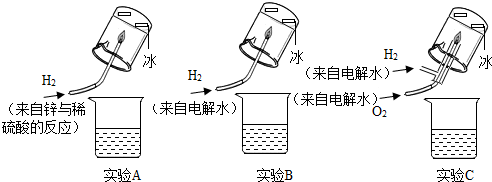
小亮取4只试管,分别加入5滴酸性KMnO4溶液,再加入小明收集的液体产物和蒸馏水,测定恰好使紫色退去所需要的液体体积.
【得出结论】
(1)用锌与稀H2SO4反应制取氢气的化学方程式是Zn+H2SO4=ZnSO4+H2↑.
(2)实验④的实验目的是对照实验.
(3)由实验①、②、③的现象可知,氢气燃烧有(填“有”或“无”)过氧化氢生成.
(4)对比实验①和②可知,用锌粒与稀H2SO4反应制得氢气不纯(填“纯”或“不纯”).
(5)实验③比实验②更接近事实,因为它可排除空气中其他成分的干扰.
【反思与评价】
“用锌和稀H2SO4反应制氢气”与“电解水制氢气.氧气”,分别进行试验①和试验③,各自的优、缺点是:前者易于操作;后者反应物、生成物纯净(氢气、氧气和水)后者原子利用率高于前者(后者电解水产生的氢气和氧气恰好完全反应,而前者制氢气时产物还有硫酸锌,点燃时消耗空气中氧气).
【提出猜想】氢气在空气中燃烧可能生成过氧化氢
【查阅资料】①过氧化氢能使紫色酸性KMnO4溶液褪色;②锌粒与稀H2SO4反应制取氢气可能混有使酸性高锰酸钾溶液褪色的物质.
【设计并完成实验】小明设计了下图所示三套实验装置,点燃氢气并收集液体燃烧物.

小亮取4只试管,分别加入5滴酸性KMnO4溶液,再加入小明收集的液体产物和蒸馏水,测定恰好使紫色退去所需要的液体体积.
| 实验序号 | 加入液体 | 实验现象 |
| ① | 实验A 的收集液4.0mL | 褪色 |
| ② | 实验B 的收集液5.5mL | 褪色 |
| ③ | 实验C的收集液10.0mL | 不褪色 |
| ④ | 蒸馏水10.0mL | 不褪色 |
(1)用锌与稀H2SO4反应制取氢气的化学方程式是Zn+H2SO4=ZnSO4+H2↑.
(2)实验④的实验目的是对照实验.
(3)由实验①、②、③的现象可知,氢气燃烧有(填“有”或“无”)过氧化氢生成.
(4)对比实验①和②可知,用锌粒与稀H2SO4反应制得氢气不纯(填“纯”或“不纯”).
(5)实验③比实验②更接近事实,因为它可排除空气中其他成分的干扰.
【反思与评价】
“用锌和稀H2SO4反应制氢气”与“电解水制氢气.氧气”,分别进行试验①和试验③,各自的优、缺点是:前者易于操作;后者反应物、生成物纯净(氢气、氧气和水)后者原子利用率高于前者(后者电解水产生的氢气和氧气恰好完全反应,而前者制氢气时产物还有硫酸锌,点燃时消耗空气中氧气).