题目内容
 实验中学兴趣小组同学,利用氢氧化钠和稀盐酸反应探究酸碱中和反应,右图是兴趣小组的同学绘制的溶液液的pH与加入的A溶液的关系图象,请你跟图象回答下列问题:
实验中学兴趣小组同学,利用氢氧化钠和稀盐酸反应探究酸碱中和反应,右图是兴趣小组的同学绘制的溶液液的pH与加入的A溶液的关系图象,请你跟图象回答下列问题:(1)该实验中发生反应的化学方程式为
(2)物质A的化学式为
(3)图中a点表示的意义为
(4)图中处于b点的溶液中溶质的化学式为
考点:中和反应及其应用,溶液的酸碱性与pH值的关系,书写化学方程式、文字表达式、电离方程式
专题:常见的酸 酸的通性
分析:(1)盐酸和氢氧化钠溶液反应生成了氯化钠和水,可以据此写出该反应的化学方程式;
(2)盐酸呈酸性,而氢氧化钠溶液呈碱性,根据图中信息可以知道起始溶液呈酸性,所以可以据此解答该题;
(3)从图中可以判断a点时pH=7,溶液呈中性,说明加入的氢氧化钠溶液与稀盐酸恰好完全反应;
(4)从图中可以判断b点时,溶液呈碱性,即加入的盐酸量不足,所以溶液中的溶质为氢氧化钠和氯化钠,可以据此解答该题;
(2)盐酸呈酸性,而氢氧化钠溶液呈碱性,根据图中信息可以知道起始溶液呈酸性,所以可以据此解答该题;
(3)从图中可以判断a点时pH=7,溶液呈中性,说明加入的氢氧化钠溶液与稀盐酸恰好完全反应;
(4)从图中可以判断b点时,溶液呈碱性,即加入的盐酸量不足,所以溶液中的溶质为氢氧化钠和氯化钠,可以据此解答该题;
解答:解:
(1)氢氧化钠和盐酸反应的化学方程式为:NaOH+HCl=NaCl+H2O;
(2)盐酸呈酸性,而氢氧化钠溶液呈碱性,根据图中信息可以知道起始溶液呈酸性,所以可以判断是将氢氧化钠溶液滴入稀盐酸中;
(3)从图中可以判断a点时pH=7,溶液呈中性,说明加入的氢氧化钠溶液与稀盐酸恰好完全反应;
(4)从图中可以判断b点时,溶液呈碱性,即加入的盐酸量不足,而氢氧化钠和盐酸反应生成了氯化钠,所以此时溶液中的溶质为:氯化钠和氢氧化
答案:
(1)NaOH+HCl=NaCl+H2O
(2)NaOH
(3)加入的氢氧化钠溶液与稀盐酸恰好完全反应
(4)NaCl、NaOH
(1)氢氧化钠和盐酸反应的化学方程式为:NaOH+HCl=NaCl+H2O;
(2)盐酸呈酸性,而氢氧化钠溶液呈碱性,根据图中信息可以知道起始溶液呈酸性,所以可以判断是将氢氧化钠溶液滴入稀盐酸中;
(3)从图中可以判断a点时pH=7,溶液呈中性,说明加入的氢氧化钠溶液与稀盐酸恰好完全反应;
(4)从图中可以判断b点时,溶液呈碱性,即加入的盐酸量不足,而氢氧化钠和盐酸反应生成了氯化钠,所以此时溶液中的溶质为:氯化钠和氢氧化
答案:
(1)NaOH+HCl=NaCl+H2O
(2)NaOH
(3)加入的氢氧化钠溶液与稀盐酸恰好完全反应
(4)NaCl、NaOH
点评:要想解答好这类题目,首先,要理解和熟记中和反应及其应用等相关知识.然后,根据所给的实验、问题情景或图表信息等,结合所学的相关知识和技能,细致地分析题意并细心地探究、推理后,按照题目要求进行认真地选择或解答即可.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
如图表示的物质变化中,属于化学变化的是( )
A、 石蜡熔化 |
B、 活性炭净水 |
C、 汽车尾气处理 |
D、 干冰人工降雨 |
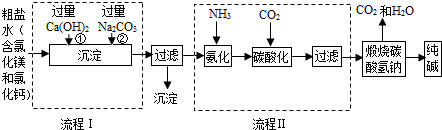

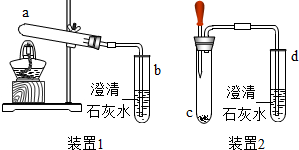 制作馒头时常加入泡打粉,在制作过程中由于产生二氧化碳气体,使馒头变得松软可口.小明对泡打粉的发面原理产生兴趣,进行了以下实验探究.
制作馒头时常加入泡打粉,在制作过程中由于产生二氧化碳气体,使馒头变得松软可口.小明对泡打粉的发面原理产生兴趣,进行了以下实验探究.