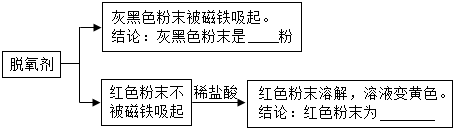
题目内容
溶液在日常生活及工农业生产上具有广泛的用途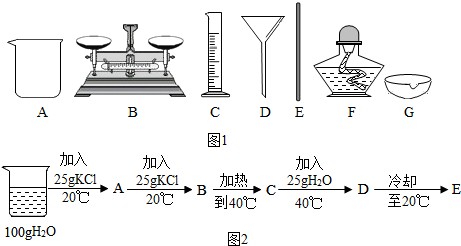
(1)医疗上常用0.9%NaCl溶液作生理盐水,生理盐水中的溶质是 .
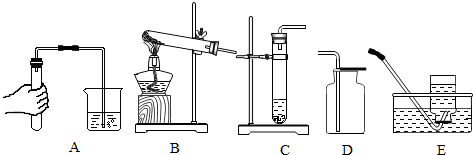
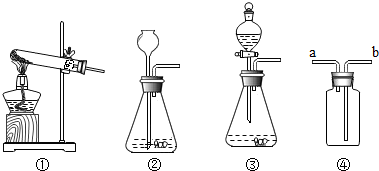
(2)配制500g生理盐水,需要的仪器为 (填序号).
(3)已知KCl的溶解度20°C时为34g,40°C时为40g.某实验小组做了如图2实验.
①B所得溶液中溶质与溶剂的质量比为 ;
②A~E所得溶液中,没有固体剩余的饱和溶液是 (填序号,下同),溶质的质量分数相等的是 .

(1)医疗上常用0.9%NaCl溶液作生理盐水,生理盐水中的溶质是
(2)配制500g生理盐水,需要的仪器为
(3)已知KCl的溶解度20°C时为34g,40°C时为40g.某实验小组做了如图2实验.
①B所得溶液中溶质与溶剂的质量比为
②A~E所得溶液中,没有固体剩余的饱和溶液是
考点:溶液、溶质和溶剂的相互关系与判断,一定溶质质量分数的溶液的配制,饱和溶液和不饱和溶液,溶质的质量分数
专题:溶液、浊液与溶解度
分析:(1)从生理盐水中有氯化钠和水去分析解答;
(2)从配制500g生理盐水的步骤及每一步需要的仪器去分析解答;
(3)从饱和溶液和不饱和溶液中溶质与溶剂的关系去分析解答.
(2)从配制500g生理盐水的步骤及每一步需要的仪器去分析解答;
(3)从饱和溶液和不饱和溶液中溶质与溶剂的关系去分析解答.
解答:解:(1)生理盐水中有氯化钠和水,其中氯化钠是固体,水是液体,所以氯化钠是溶质;
故答案为:NaCl
(2)配制500g生理盐水,需要用托盘天平称量500g×0.9%=4.5g的食盐,和用量筒量取495.5ml的水,并把食盐和水放在烧杯里溶解,并作玻璃棒进行搅拌;故答案为:ABCE;、
(3)①已知KCl的溶解度20℃时为34g.其含义为:在20℃时在100g水里,最多能溶解34g氯化钾;
在A中,由于氯化钾的质量25g<34g,此时所得溶液为不饱和溶液,溶质的质量为:
×100%=20%;
在B中,溶质质量为25g+25g=50g,但在20℃在100g水里,最多能溶解34g氯化钾,此时溶质有剩余:50g-34g=16g,因此溶液中的溶质与溶剂的质量比为:34g:100g=17:50;溶质的质量分数为:
×100%=25.4%;
在C中在40℃时,此时由于氯化钾的溶解度为40g,C中的溶质仍有剩余(50g-40g=10g);溶质的质量分数为:
×100%=28.6%;
在D中设125g水中最多溶解氯化钾的质量为X,
40g/100g=X/125g;解之得:X=50g;故此时溶液恰好饱和;
溶质的质量分数为:
×100%=28.6%
在E中当冷却到20℃时,100g水中最多可溶解34氯化钾,由于溶液具有均一性,所以125g水中最多可溶解42.5g,此时为饱和溶液,故溶质的质量分数为:
×100%=25.4%;
②由上面①的分析可知答案为:D B与E和C与D.
故答案为:NaCl
(2)配制500g生理盐水,需要用托盘天平称量500g×0.9%=4.5g的食盐,和用量筒量取495.5ml的水,并把食盐和水放在烧杯里溶解,并作玻璃棒进行搅拌;故答案为:ABCE;、
(3)①已知KCl的溶解度20℃时为34g.其含义为:在20℃时在100g水里,最多能溶解34g氯化钾;
在A中,由于氯化钾的质量25g<34g,此时所得溶液为不饱和溶液,溶质的质量为:
| 25g |
| 25g+100g |
在B中,溶质质量为25g+25g=50g,但在20℃在100g水里,最多能溶解34g氯化钾,此时溶质有剩余:50g-34g=16g,因此溶液中的溶质与溶剂的质量比为:34g:100g=17:50;溶质的质量分数为:
| 34g |
| 100g+34g |
×100%=25.4%;
在C中在40℃时,此时由于氯化钾的溶解度为40g,C中的溶质仍有剩余(50g-40g=10g);溶质的质量分数为:
| 40g |
| 100g+40g |
在D中设125g水中最多溶解氯化钾的质量为X,
40g/100g=X/125g;解之得:X=50g;故此时溶液恰好饱和;
溶质的质量分数为:
| 50g |
| 50g+125g |
在E中当冷却到20℃时,100g水中最多可溶解34氯化钾,由于溶液具有均一性,所以125g水中最多可溶解42.5g,此时为饱和溶液,故溶质的质量分数为:
| 42.5g |
| 125g+42.5g |
②由上面①的分析可知答案为:D B与E和C与D.
点评:计算溶质质量分数时剩余的溶质不能参与计算.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列图示的实验中涉及到化学变化的是( )
A、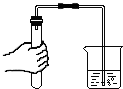 检查装置气密性 |
B、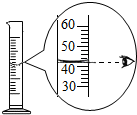 读取水的体积 |
C、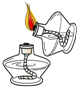 点燃酒精灯 |
D、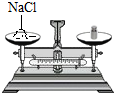 称NaCl的质量 |
 实验中学兴趣小组同学,利用氢氧化钠和稀盐酸反应探究酸碱中和反应,右图是兴趣小组的同学绘制的溶液液的pH与加入的A溶液的关系图象,请你跟图象回答下列问题:
实验中学兴趣小组同学,利用氢氧化钠和稀盐酸反应探究酸碱中和反应,右图是兴趣小组的同学绘制的溶液液的pH与加入的A溶液的关系图象,请你跟图象回答下列问题: