题目内容
煤是社会生产、生活中最重要的能源,工业上常把煤进行气化和液化处理,使煤变成清洁能源.煤气化和液化的流程示意图如下:

(1)第①步操作发生的是 (选填“物理”或“化学”)变化.
(2)第②步是精炼煤与水蒸气的反应,化学方程式为 .
(3)第③步反应属于 (填基本反应类型).
(4)含硫化合物洗液经过提炼后,可用来制硫酸,过程是:含硫化合物氧化得到SO2,SO2进一步氧得到SO3,测定SO3与水反应后溶液pH的操作方法是 .
(5)从“绿色化学”的角度分析,“煤的气化和煤的液化”生产流程的优点是 .

(1)第①步操作发生的是
(2)第②步是精炼煤与水蒸气的反应,化学方程式为
(3)第③步反应属于
(4)含硫化合物洗液经过提炼后,可用来制硫酸,过程是:含硫化合物氧化得到SO2,SO2进一步氧得到SO3,测定SO3与水反应后溶液pH的操作方法是
(5)从“绿色化学”的角度分析,“煤的气化和煤的液化”生产流程的优点是
考点:化石燃料及其综合利用,溶液的酸碱度测定,化学变化和物理变化的判别,反应类型的判定,书写化学方程式、文字表达式、电离方程式
专题:化学与能源
分析:(1)根据变化的特征分析变化的类型;
(2)根据煤与水蒸气的反应,写出反应的方程式;
(3)根据反应的特点,分析反应的类型;
(4)根据pH试纸的使用方法分析回答;
(5)根据原料的利用和对环境的影响分析回答.
(2)根据煤与水蒸气的反应,写出反应的方程式;
(3)根据反应的特点,分析反应的类型;
(4)根据pH试纸的使用方法分析回答;
(5)根据原料的利用和对环境的影响分析回答.
解答:解:(1)第①步操作中没有新物质生成,发生的是物理变化.
(2)第②步是精炼煤与水蒸气的反应,在高温条件下生成了氢气和一氧化碳.反应化学方程式为:H2O+C
H2+CO.
(3)第③步反应是氢气和一氧化碳在催化剂的作用下生成了甲醇,由两种物质生成了一种物质,属于化合 反应.
(4)测定SO3与水反应后溶液pH的操作方法是:在玻璃片上放一小片pH试纸,用玻璃棒把待测液滴在pH试纸上,然后把试纸显示的颜色与标准比色卡对照,读出溶液的pH.
(5)从“绿色化学”的角度分析,“煤的气化和煤的液化”生产流程的优点是:原料全部转化为产品或实现“零排放”,不对环境造成污染.
故答为:(1)物理;(2)H2O+C
H2+CO;(3)化合反应;(4)在玻璃片上放一小片pH试纸,用玻璃棒把待测液滴在pH试纸上,然后把试纸显示的颜色与标准比色卡对照,读出溶液的pH;(5)原料全部转化为产品或实现“零排放”,不对环境造成污染.
(2)第②步是精炼煤与水蒸气的反应,在高温条件下生成了氢气和一氧化碳.反应化学方程式为:H2O+C
| ||
(3)第③步反应是氢气和一氧化碳在催化剂的作用下生成了甲醇,由两种物质生成了一种物质,属于化合 反应.
(4)测定SO3与水反应后溶液pH的操作方法是:在玻璃片上放一小片pH试纸,用玻璃棒把待测液滴在pH试纸上,然后把试纸显示的颜色与标准比色卡对照,读出溶液的pH.
(5)从“绿色化学”的角度分析,“煤的气化和煤的液化”生产流程的优点是:原料全部转化为产品或实现“零排放”,不对环境造成污染.
故答为:(1)物理;(2)H2O+C
| ||
点评:本题通过煤的综合利用,考查了物质的变化、方程式的书写、反应的类型的判断等知识,属于基础的知识,难度不大.根据已有的知识即可解答.、

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目

 向盛有45g蒸馏水的烧杯中加入含氯化钠的氢氧化钠固体混合物5g,使之全部溶解后,向烧杯中
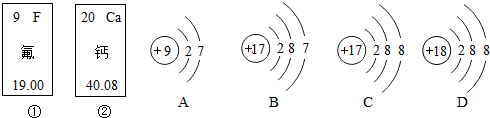
向盛有45g蒸馏水的烧杯中加入含氯化钠的氢氧化钠固体混合物5g,使之全部溶解后,向烧杯中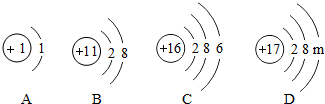 如图是A、B、C、D四种粒子的结构示意图,回答下列问题:
如图是A、B、C、D四种粒子的结构示意图,回答下列问题: