题目内容
5.利用下列仪器进行气体的制取实验.请根据要求填空.
①图1中仪器A的名称是锥形瓶.
②实验室加热氯酸钾与二氧化锰混合物制取氧气,并用排水法收集一瓶氧气,选择图1中的仪器G、I外,还需要仪器BF(填字母,夹持装置略)组合装置.开始收集氧气的最佳时机是有连续均匀的气泡冒出时.
③若要用块状大理石和稀盐酸制取并收集一瓶CO2,并随时控制反应发生或停止,应选择图1中的仪器BDEH(填字母,夹持装置略)组合装置,反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.
④若用图2所示装置检验制取的二氧化碳气体中是否含有氯化氢和水蒸气,请写出气体通过装置的接口顺序dab(或dcab)(用“a”、“b”、“c”、“d”表示).

⑤用对比实验方法探究二氧化碳的性质.实验中振荡三个软塑料瓶(见图3),观察到塑料瓶变瘪的程度大小为A瓶>B瓶>C瓶,其中石灰水变浑浊的瓶内发生反应的化学方程式为Ca(OH)2+CO2═CaCO3↓+H2O;对比A瓶与C(选填“B”或“C”)瓶的实验现象,可证明CO2能与NaOH发生反应.
分析 ①据常用仪器的名称解答;
②实验室加热氯酸钾与二氧化锰混合物制取氧气的氧气装置为固体加热型,可用排水法收集分析;
③制取并收集二氧化碳时,制取装置为固液常温型,
④检验物质时,应先检验水蒸气后检验氯化氢气体,否则通过溶液会带出水蒸气,就无法检验是否有水了,检验或除杂在通过洗气瓶的时候应长进短出;
⑤根据二氧化碳与氢氧化钠、氢氧化钙、水的反应进行分析;
解答 解:①图1中仪器A的名称是锥形瓶;
②实验室加热氯酸钾与二氧化锰混合物制取氧气,并用排水法收集一瓶氧气,选择图1中的仪器G、I外,还需要仪器试管、铁架台、导管等;开始收集氧气的最佳时机是导管口有均匀连续气泡冒出时;
③若要用块状大理石制取并收集一瓶CO2,将块状大理石放在有空塑料板上,能随时控制反应的发生和停止,反应为固液常温型,应选择图1中的仪器BDEH;反应的方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
④若用图2装置检验制取的二氧化碳气体中是否含有氯化氢和水蒸气,气体通过装置的接口顺序是c、d、b、a,或d、c、b、a;
⑤实验三中可观察到三个软塑料瓶变瘪的程度大小为A>B>C,A瓶内发生反应为二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,化学方程式为:CO2+2NaOH═Na2CO3+H2O,对比A瓶与C瓶的实验现象可证明CO2 能与NaOH发生反应;.
故答案为:①锥形瓶;②B F、有连续均匀的气泡冒出时;③B D E H、CaCO3+2HCl═CaCl2+H2O+CO2↑;④c d a b (或d c a b);
⑤Ca(OH)2+CO2═CaCO3↓+H2O、C.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

 阅读快车系列答案
阅读快车系列答案| A. | 玉堂陈醋是混合物,它的有效成分是醋酸 | |
| B. | 醋酸有2个碳原子、4个氢原子和2个氧原子构成 | |
| C. | 醋酸是由碳、氢、氧三种元素组成的化合物,其元素个数比为1:2:1 | |
| D. | 醋酸是一种有机物 |
| A. | 氮气的化学性质稳定可作保护气 | B. | 氧气有助燃性可作燃料 | ||
| C. | 室内燃气泄漏应立即打开排风扇 | D. | 用过滤的方法将硬水转化成软水 |
| A. | 用稀硫酸清除铁锈 | |
| B. | 服用含氢氧化铝的药物治疗胃酸过多 | |
| C. | 用熟石灰改良酸性土壤 | |
| D. | 用氢氧化钠溶液洗涤石油产品中残留硫酸 |
| A. |  吸取液体药品 | B. |  加热液体 | C. |  测溶液的pH | D. |  稀释浓硫酸 |
| A. | 开灯检查泄漏情况 | B. | 迅速关闭阀门,打开门窗通风 | ||
| C. | 打开抽油烟机排出泄漏的气体 | D. | 在房间里放一盆水吸收泄漏的气体 |
 甲、乙、丙三种不含结晶水的固体物质的溶解度曲线如图.下列说法中正确的是( )
甲、乙、丙三种不含结晶水的固体物质的溶解度曲线如图.下列说法中正确的是( )| A. | 甲的溶解度比乙大 | |
| B. | t1℃时,将等质量的乙、丙分别配成饱和溶液,所得溶液质量:乙>丙 | |
| C. | 将甲、丙的饱和溶液分别由t1℃升温到t2℃,两种溶液中溶质的质量分数相等 | |
| D. | 将t3℃时甲、乙、丙的饱和溶液分别恒温蒸发等量的水,析出溶质的质量:甲>乙>丙 |
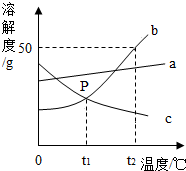 根据图中a、b、c三种物质的溶解度曲线,回答下列问题:
根据图中a、b、c三种物质的溶解度曲线,回答下列问题: