题目内容
3.下列物质按照酸、碱、盐、氧化物顺序排列的是( )| A. | K2SO4 Ba(OH)2 KCl KClO3 | B. | HNO3 NaOH HCl CuO | ||
| C. | HCl Ca(OH)2 AgCl NO2 | D. | H2SO4 KNO3 NH4Cl CH4 |
分析 根据物质的组成进行分析,氧化物是指由两种元素组成其中一种是氧元素的化合物,酸是指电离时生成的阳离子全部是氢离子的化合物,碱是指电离时生成的阴离子全部是氢氧根离子的化合物,盐是指由金属离子和酸根离子组成的化合物.
解答 解:A、K2SO4是盐;Ba(OH)2属于碱;KCl是盐;KClO3是盐,故错误;
B、HNO3属于酸;NaOH是碱;HCl是酸;CuO是氧化物,故错误;
C、HCl是酸;Ca(OH)2是碱;AgCl属于盐;NO2是氧化物,故正确;
D、H2SO4是酸;KNO3是盐;NH4Cl是盐;CH4是有机物,不属于酸、碱、盐和氧化物,故错误.
故选C.
点评 本题考查了常见物质的类别,完成此题,可以依据物质的组成进行.

练习册系列答案
 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
7.下列说法错误的是( )
| A. | 月饼盒中放入装有铁粉的小包装,可以防止月饼变质 | |
| B. | 液化气泄漏时,应首先关闭阀门,打开门窗换气 | |
| C. | 车船表面喷涂油漆,可防止生锈 | |
| D. | 煤、石油、煤气是三大重要的化石燃料 |
8.分子、原子、离子等都是构成物质的微粒.下列物质由离子构成的是( )
| A. | 干冰 | B. | 镁 | C. | 金刚石 | D. | 氯化钠 |
11.干燥剂的干燥性能可用干燥效率(1m3空气中实际余留水蒸气的质量)来衡量.某些干燥剂的干燥效率数据如下表所示.根据表中数据作出的推测不合理的是( )
| 物质 | CaCl2 | CaBr2 | CaO | CaSO4 | MgO | Al2O3 | ZnCl2 | ZnBr2 | CuSO4 |
| 干燥效率 | 0.14 | 0.14 | 0.2 | 0.04 | 0.008 | 0.003 | 0.8 | 1.1 | 1.4 |
| A. | MgO的干燥性能比CaO好 | |
| B. | 干燥剂中金属元素对干燥效率影响可能比较大 | |
| C. | MgSO4的干燥效率可能小于0.04 | |
| D. | 干燥剂中非金属元素对干燥效率无影响 |
18.下列各组物质,按单质、氧化物、混合物顺序排列的是( )
| A. | 炭、氯酸钾、石油 | B. | 钢、氧化镁、铁锈 | ||
| C. | 臭氧、二氧化硫、冰水混合物 | D. | 液态氧、干冰、空气 |
12.环保部门测定某雨水中含有亚硫酸(H2SO3),雨水的pH变化如下表所示.已知该酸不稳定,且比硫酸酸性弱,在空气中易发生反应:2H2SO3+O2=2H2SO4.下列说法不正确的是( )
| 测定时间/分钟 | 1 | 2 | 3 | 4 | 5 |
| pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
| A. | 酸雨可腐蚀某些金属制品 | |
| B. | 雨水酸性逐渐减弱 | |
| C. | 主要是因为雨水中的成分发生变化,溶液pH发生变化 | |
| D. | 酸雨主要是因为空气受到SO2及氮氧化物的污染形成的 |
 如图所示装置的U形管左侧内固定一支小试管.
如图所示装置的U形管左侧内固定一支小试管. 化学反应前后原子的种类和数目不变; 此过程中不变的粒子是碳原子,氧原子,氮原子.
化学反应前后原子的种类和数目不变; 此过程中不变的粒子是碳原子,氧原子,氮原子.
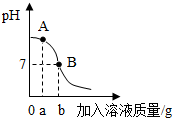 如图是稀HCl和NaOH溶液反应的pH变化曲线图,从图中可以看出该实验中是将稀盐酸滴入氢氧化钠溶液;当加入溶液质量是ag时,此时混合溶液中溶质为氯化钠和氢氧化钠;反应的化学方程式是NaOH+HCl=NaCl+H2O.
如图是稀HCl和NaOH溶液反应的pH变化曲线图,从图中可以看出该实验中是将稀盐酸滴入氢氧化钠溶液;当加入溶液质量是ag时,此时混合溶液中溶质为氯化钠和氢氧化钠;反应的化学方程式是NaOH+HCl=NaCl+H2O.