题目内容
13.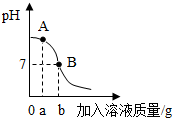 如图是稀HCl和NaOH溶液反应的pH变化曲线图,从图中可以看出该实验中是将稀盐酸滴入氢氧化钠溶液;当加入溶液质量是ag时,此时混合溶液中溶质为氯化钠和氢氧化钠;反应的化学方程式是NaOH+HCl=NaCl+H2O.
如图是稀HCl和NaOH溶液反应的pH变化曲线图,从图中可以看出该实验中是将稀盐酸滴入氢氧化钠溶液;当加入溶液质量是ag时,此时混合溶液中溶质为氯化钠和氢氧化钠;反应的化学方程式是NaOH+HCl=NaCl+H2O.
分析 根据坐标变化的趋势结合盐酸的pH小于7,氢氧化钠溶液的pH大于7分析;当加入溶液的质量为ag时,溶液呈现碱性来分析.
解答 解:由图象可以看出,开始时溶液的pH大于7,呈碱性,随后pH逐渐减小,表明是向氢氧化钠溶液中加入的稀盐酸,故该实验是将盐酸滴加到氢氧化钠的过程;当加入溶液质量是ag时,溶液的pH大于7,呈碱性,说明氢氧化钠过量,因此溶液中的溶质为氯化钠和氢氧化钠;盐酸与氢氧化钠发生中和反应生成氯化钠和水.
故填:稀盐酸;氢氧化钠溶液;氯化钠和氢氧化钠;NaOH+HCl=NaCl+H2O.
点评 本题以图象的形式考查了酸碱中和反应时溶液pH的变化,以及物质间的反应关系,完成此题,可以依据已有的知识进行,难度不大.

练习册系列答案
相关题目
3.下列物质按照酸、碱、盐、氧化物顺序排列的是( )
| A. | K2SO4 Ba(OH)2 KCl KClO3 | B. | HNO3 NaOH HCl CuO | ||
| C. | HCl Ca(OH)2 AgCl NO2 | D. | H2SO4 KNO3 NH4Cl CH4 |
4.下列有关空气中某些成分的说法在,不正确的是( )
| A. | 氧气可用于医疗急救 | B. | 空气的主要成分是氮气和氧气 | ||
| C. | 新鲜空气中不含二氧化碳 | D. | 食品包装袋中充入氮气以防腐 |
1.下列化学反应中,无明显现象的是( )
| A. | 氢氧化钠溶液和稀硫酸 | B. | 氧化铁和稀盐酸 | ||
| C. | 氧化钙和水 | D. | 碳酸钠和稀盐酸 |
8.下列各种物质中,都是由离子构成的一组是( )
| A. | 铁和铜 | B. | 氯化钠和硫酸铜 | C. | 水和二氧化碳 | D. | 氧气和氢气 |
18.分类法是化学学习和研究的重要方法之一.下列分类正确的是( )
| A. | 有机物:葡萄糖、醋酸、碳酸 | B. | 碱:烧碱、纯碱、氨水 | ||
| C. | 混合物:生铁、生石灰、石油 | D. | 盐:氯化钙、硫酸钠、小苏打 |
3.下列情况不会污染空气的是( )
| A. | 人和动物的呼吸 | B. | 焚烧塑料垃圾 | C. | 工厂的废气 | D. | 汽车排放的尾气 |
