题目内容
18. 如图是甲、乙两物质的溶解度曲线,以下说法正确的是( )
如图是甲、乙两物质的溶解度曲线,以下说法正确的是( )| A. | 甲物质的溶解度大于乙物质的溶解度 | |
| B. | t2℃时,150g甲物质的溶液中含50g甲 | |
| C. | t1℃时,甲、乙两种物质的饱和溶液中,溶质的质量相等 | |
| D. | t2℃时,配制相同质量的甲、乙饱和溶液,乙需要水的质量多 |
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:A、在一定的温度下比较物质的溶解度,没有指明温度,不能直接比较,错误;
B、t2℃时,150g甲物质的饱和溶液中含50g甲,错误;
C、t1℃时,等质量的甲、乙两种物质的饱和溶液中,溶质的质量相等,错误;
D、2℃时,配制相同质量的甲、乙饱和溶液,乙需要水的质量多,正确;
故选D.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
8.除去下列各组物质中的杂质,所用试剂和方法均正确的是( )
| 物质 | 杂质 | 除杂所用试剂和方法 | |
| A | H2 | 水蒸气 | 将气体通过浓硫酸 |
| B | CO2 | CO | 将气体在氧气中点燃 |
| C | Fe | Mg | 加入足量的稀硫酸,过滤 |
| D | CaO | CaCO3 | 加入适量的稀盐酸,蒸发 |
| A. | A | B. | B | C. | C | D. | D |
3.下列选项中物质的俗名、化学式、类别、用途完全对应的是( )
| A. | 天然气 CH4有机物 燃料 | |
| B. | 生石灰 CaO 氧化物 补钙剂 | |
| C. | 小苏打 NaHCO3盐 发酵粉 | |
| D. | 酒精 C2H5OH碱 溶剂 |
10.(1)实验室制得的二氧化碳中常含有水蒸气和少量酸 雾,为了获得纯净的二氧化碳可选用如图中的C套装置来净化.
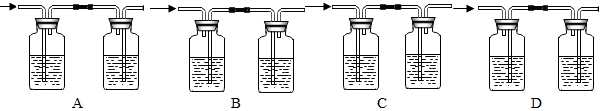
其中左瓶中应盛碳酸氢钠溶液;右瓶中应盛浓硫酸.
(2)向氢氧化钠溶液中通入适量二氧化碳后,仅使溶液中 50%的氢氧化钠反应,反应后溶液中 CO${\;}_{3}^{2-}$和 OH的个数比为1:2.
(3)现将石灰石样品 15g 与 105.4g 稀盐酸放入烧杯中充分反应(杂质不溶于水也不与稀 盐酸反应),反应时间与反应前后烧杯内物质的质量变化如表所示:
请计算回答:①样品中碳酸钙的质量分数.(计算结果保留 1 位小数)
②反应后所得溶液中溶质的质量分数.

其中左瓶中应盛碳酸氢钠溶液;右瓶中应盛浓硫酸.
(2)向氢氧化钠溶液中通入适量二氧化碳后,仅使溶液中 50%的氢氧化钠反应,反应后溶液中 CO${\;}_{3}^{2-}$和 OH的个数比为1:2.
(3)现将石灰石样品 15g 与 105.4g 稀盐酸放入烧杯中充分反应(杂质不溶于水也不与稀 盐酸反应),反应时间与反应前后烧杯内物质的质量变化如表所示:
| 反应时间/s | 20 | 40 | 60 | 80 | 100 | 120 |
| 质量/g | 119.52 | 118.64 | 117.76 | 116.88 | 116 | 116 |
②反应后所得溶液中溶质的质量分数.
7.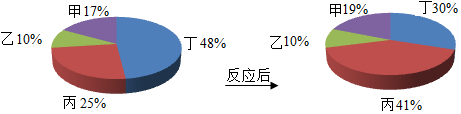 甲、乙、丙、丁四种物质在一定条件下混合反应,一段时间后,测得各物质的质量分数变化如图所示,则有关说法正确的是( )
甲、乙、丙、丁四种物质在一定条件下混合反应,一段时间后,测得各物质的质量分数变化如图所示,则有关说法正确的是( )
 甲、乙、丙、丁四种物质在一定条件下混合反应,一段时间后,测得各物质的质量分数变化如图所示,则有关说法正确的是( )
甲、乙、丙、丁四种物质在一定条件下混合反应,一段时间后,测得各物质的质量分数变化如图所示,则有关说法正确的是( )| A. | 该反应属于分解反应 | |
| B. | 乙一定是该反应的催化剂 | |
| C. | 丁是单质 | |
| D. | 该反应生成甲和丙的质量比为19:41 |
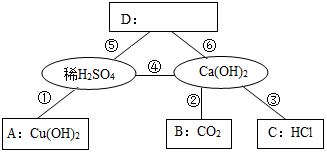
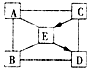 A~E是初中常见的物质:盐酸、氢氧化钠、氢氧化钙、碳酸钠、二氧化碳中的某一种.A可用于金属表面除锈,B可用来改良酸性土壤.它们相互间发生反应或转化的关系如图所示(“-”表示两种物质间能发生反应,“→”表示两种物质间的转化关系).
A~E是初中常见的物质:盐酸、氢氧化钠、氢氧化钙、碳酸钠、二氧化碳中的某一种.A可用于金属表面除锈,B可用来改良酸性土壤.它们相互间发生反应或转化的关系如图所示(“-”表示两种物质间能发生反应,“→”表示两种物质间的转化关系).