题目内容
2.向80g溶质质量分数为15%的氢氧化钠溶液中滴加某溶质质量分数的稀盐酸,在滴加过程中溶液pH 值随所加稀盐酸的量的变化如图所示,试求: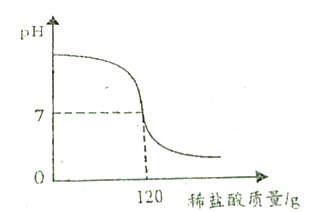
(1)当酸碱恰好中和时,生成的氯化钠的质量;
(2)所加稀盐酸的溶质质量分数(计算结果精确到0.1%)
分析 稀盐酸与氢氧化钠溶液反应生成氯化钠和水,由图示可知,当酸碱恰好中和时消耗的稀盐酸的质量为120g,由参加反应的氢氧化钠溶液的质量、溶质的质量分数,由反应的化学方程式列式计算出当酸碱恰好中和时,生成的氯化钠的质量、所加稀盐酸的溶质的质量分数.
解答 解:(1)80g溶质质量分数为15%的氢氧化钠溶液中含溶质的质量为:80g×15%=12g.
设生成氯化钠的质量为x,参加反应的稀盐酸中溶质的质量为y
HCl+NaOH═NaCl+H2O
36.5 40 58.5
y 12g x
$\frac{36.5}{y}=\frac{40}{12g}=\frac{58.5}{x}$
解得:x=17.55g y=10.95g
(2)所加稀盐酸的溶质的质量分数为:$\frac{10.95g}{120g}×100%$≈9.1%.
答:(1)当酸碱恰好中和时,生成的氯化钠的质量17.55g,(2)所加稀盐酸溶液的溶质的质量分数为9.1%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.下列实验操作中,能达到实验目的是( )
| A. |  干燥氨气 | B. |  测定某溶液的pH | ||
| C. |  向试管中倾倒液体 | D. | 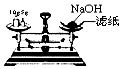 称取氢氧化钠固体 |
13.已知某两种物质在一定条件下发生化学反应,其微观示意图如下,下列说法正确的是( )
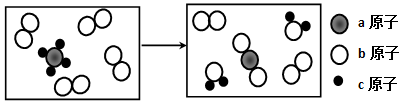

| A. | 反应前后分子的种类、个数都发生改变 | |
| B. | 该反应不是置换反应 | |
| C. | 参加反应的两种分子的个数比为4:1 | |
| D. | 该反应中生成物有单质和化合物 |
7.下列物质的主要成分与化学式相符合的是( )
| A. | 纯碱NaOH | B. | 天然气CO | C. | 石灰石Ca(OH)2 | D. | 小苏打NaHCO3 |
14.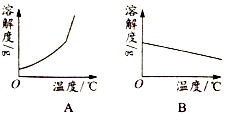 如表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题
如表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题
(1)依据如表数据,绘制Ca(OH)2和NaOH的溶解度曲线,如图中能表示NaOH溶解度曲线的是A(填“A”或“B”).
(2)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,可采取措施有①②(填序号).
①蒸发水 ②升高温度 ③降低温度 ④加入水
(3)现有60℃时含有Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是降温结晶.
(4)根据表中数据可知Ca(OH)2属于微溶(填“易溶、可溶、微溶或难溶”)物质.
 如表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题
如表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
(2)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,可采取措施有①②(填序号).
①蒸发水 ②升高温度 ③降低温度 ④加入水
(3)现有60℃时含有Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是降温结晶.
(4)根据表中数据可知Ca(OH)2属于微溶(填“易溶、可溶、微溶或难溶”)物质.
11.下列反应中属于置换反应的是( )
| A. | C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2 | B. | 2Na2O2+2CO2═2Na2CO2+O2 | ||
| C. | 3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | D. | 2NaCl(熔融)$\frac{\underline{\;通电\;}}{\;}$2Na+Cl2↑ |
12.下列有关能源、生活、环境、资源问题叙述错误的是( )
| A. | 加速石油、煤炭的开采,快速提高人们的生活质量 | |
| B. | pH<5.6的雨水称为酸雨 | |
| C. | “温室效应”主要是由CO2等气体所引起的 | |
| D. | 生活中为降低水的硬度,常用的方法是煮沸 |