题目内容
2.一包固体粉末可能含有Mg(NO3)2、CaCO3、NaOH、CuCl2、NaCl和Ca(NO3)2中的一种或几种,为确定其组成,某同学设计了如下实验方案,下列判断正确的是( )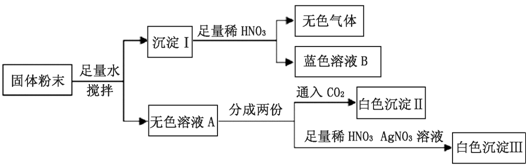
| A. | 沉淀Ⅰ是氢氧化铜沉淀 | |
| B. | 无色溶液A中一定有NaOH | |
| C. | 原固体粉末肯定有NaCl | |
| D. | 原固体粉末一定有CaCO3、NaOH、Mg(NO3)2、CuCl2和Ca(NO3)2 |
分析 根据铜离子在溶液中显蓝色,NaOH和CuCl2会生成氢氧化铜沉淀,而氢氧化铜沉淀与稀硝酸反应生成硝酸铜溶液;CaCO3和硝酸反应会生成气体等知识进行分析.
解答 解:根据“一包固体粉末可能含有Mg(NO3)2、CaCO3、NaOH、CuCl2、NaCl和Ca(NO3)2中的一种或几种”,结合图框,则推测铜离子在溶液中显蓝色,则一定有CuCl2;CaCO3和硝酸反应会生成气体,则蓝色溶液B中有硝酸铜、硝酸钙.而原固体粉末一定有CaCO3、CuCl2和Ca(NO3)2,无法确定是否含有NaCl、Mg(NO3)2.通入二氧化碳产生白色沉淀,说明溶液中一定硝酸钙,而此时必选存在氢氧根离子才能对应沉淀.因为存在氢氧化钠和氯化铜,所以溶液A一定存在一定含有钠离子和氯离子,进而后面实验对氯离子的检验没有意义,因为无法确定原固体中含有氯化钠.
故选:B.
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.

练习册系列答案
相关题目
12.把生石灰、二氧化碳、食盐分别溶于水,往它们的溶液里分别滴入紫色石蕊溶液,则上述溶液呈现的颜色依次是( )
| A. | 紫色、蓝色、红色 | B. | 红色、蓝色、蓝色 | C. | 红色、蓝色、紫色 | D. | 蓝色、红色、紫色 |
13.2017年第二十五届“世界水日”,宣传主题是“Wastewater”(废水).下列做法不会形成水污染的是( )
| A. | 工业废水直接排入大河 | B. | 使用含磷洗涤剂 | ||
| C. | 合理使用农药和化肥 | D. | 生活污水直接排入田野 |
10.分类是化学学习的重要方法之一,下列各组物质按照单质、盐、混合物顺序排列的是( )
| A. | 液氧、酸式碳酸钠、粗盐 | B. | 生铁、食盐、冰水混溶物 | ||
| C. | 青铜、高锰酸钾、石油 | D. | 钙片、氯化钠、海水 |
17.如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法正确的是( )
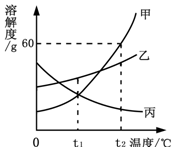

| A. | 三种固体物质的溶解度关系为甲>乙>丙 | |
| B. | t2℃100 g甲物质饱和溶液中含有60 g甲 | |
| C. | 将t1℃丙物质饱和溶液升温到t2℃可能出现浑浊现象 | |
| D. | t2℃时,三种物质的饱和溶液降温到t1℃,所得溶液溶质质量分数:乙>甲=丙 |
7.二甲醚(C2H6O)是一种应用前景广阔的清洁燃料.下列有关说法错误的是( )
| A. | 二甲醚由C、H、O三种元素组成 | |
| B. | 二甲醚属于有机化合物 | |
| C. | 二甲醚相对分子质量为46 | |
| D. | 二甲醚中碳、氢、氧元素的质量比为2:6:1 |
14.下列实验方案能达到实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 除去CO2中少量的HCl | 通入足量的氢氧化钠溶液,干燥 |
| B | 鉴别食盐水和稀盐酸 | 分别加入无色酚酞试液 |
| C | 除去Na2SO4溶液中的NaHCO3 | 加入稀盐酸至不在产生气泡为止 |
| D | 从氯酸钾与二氧化锰制氧后的固体中回收二氧化锰 | 往固体中加水溶解,过滤后对滤渣进行洗涤、烘干 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
11.2015年,中国女科学家屠呦呦因发现青蒿素(C15H22O5)而获得诺贝尔生理学或医学奖,下列有关青蒿素的说法正确的是( )
| A. | 青蒿素中氧元素的质量分数最小 | |
| B. | 青蒿素由碳、氢、氧三种原子构成 | |
| C. | 青蒿素是有机化合物 | |
| D. | 青蒿素中碳、氢、氧元素的质量比为15:22:5 |