题目内容
16.对下列物质:①纯碱 ②食盐水 ③石灰水 ④烧碱 ⑤液氧 ⑥氯酸钾,分类全部正确的是( )| A. | 碱-①④ | B. | 纯净物-①③④⑤ | C. | 氧化物-⑤⑥ | D. | 盐-①⑥ |
分析 根据碱是指在电离时产生的阴离子全部是氢氧根离子的化合物;纯净物是由一种物质组成的物质;氧化物是由两种元素组成,且其中一种是氧的化合物;盐是由金属离子(或铵根离子)和酸根离子组成的化合物,据此结合物质的组成进行分析判断.
解答 解:A、纯碱是由钠离子和碳酸根离子组成的化合物,属于盐,故选项错误.
B、石灰水是由水、氢氧化钙组成的,属于混合物,故选项错误.
C、液氧是由一种元素组成的,属于单质,故选项错误.
D、纯碱、氯酸钾都是由金属离子和酸根离子组成的化合物,都属于盐,故选项正确.
故选D.
点评 本题难度不大,考查物质类别的判别,抓住碱、盐、纯净物和混合物的特征是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.wg金属R(相对原子质量为M)与xgc%的稀硫酸恰好完全反应产生yg氢气,则反应中金属R的化合价是( )
| A. | +$\frac{M•x•c%}{98w}$ | B. | +$\frac{M•x•c%}{49w}$ | C. | +$\frac{x•c%}{w}$ | D. | +$\frac{M•y}{w}$ |
4.某化学兴趣小组为了测定镁铜合金中镁的质量分数,取出3g合金样品,将60g稀硫酸分6次加入样品中,充分反应后过滤、洗涤、干燥、称重,得到的实验数据如下:
(1)从以上数据可知,m的值为2.5g;
(2)计算整个实验过程中总共生成氢气的质量是多少?
(3)计算所用稀硫酸中H2SO4的质量分数?
| 稀硫酸用量 | 剩余固体质量 |
| 第一次加入10g | mg |
| 第二次加入10g | 2.0g |
| 第三次加入10g | 1.5g |
| 第四次加入10g | 1.0g |
| 第五次加入10g | 0.6g |
| 第六次加入10g | 0.6g |
(2)计算整个实验过程中总共生成氢气的质量是多少?
(3)计算所用稀硫酸中H2SO4的质量分数?
11.将一定质量的 a、b、c、d 四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质 量如下:
下列说法中正确的是( )
| 物质 | a | b | c | d |
| 反应前质量/g | 6.4 | 3.2 | 4.0 | 0.5 |
| 反应后质量/g | 待测 | 2.56 | 7.2 | 0.5 |
| A. | a和b是反应物,d一定是催化剂 | |
| B. | 反应后a物质的质量为4.64g | |
| C. | c 物质中元素的种类,一定等于a、b两种物质中元索的种类 | |
| D. | 若物质a与b 相对分子质量之比为2:l,则反应中a与b的化学计量数之比为3:1 |
5.为除去下列物质中的杂质(括号内是杂质),所选用的除杂试剂和分离方法都正确的是( )
| 序号 | 物质(括号内为杂质) | 除杂试剂 | 分离方法 |
| A | 硫酸铜溶液(硫酸) | 氧化铜 | 过滤 |
| B | NaOH溶液[Ca(OH)2溶液] | 二氧化碳 | 过滤 |
| C | 二氧化碳(一氧化碳) | 氢氧化钠溶液 | 洗气 |
| D | 二氧化锰粉末(碳粉) | 水 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
6. 为研究影响化学反应快慢的因素,小明选取成分相同的大理石碎屑、块状大理石两种样品各6克,分别与足量的、溶质质量分数相同的稀盐酸在锥形瓶中反应(样品中杂质不与稀盐酸反应),实验装置如右图所示.每2分钟读取一次电子天平的示数,据此计算生成的二氧化碳的质量,前18分钟数据记录见下表:
为研究影响化学反应快慢的因素,小明选取成分相同的大理石碎屑、块状大理石两种样品各6克,分别与足量的、溶质质量分数相同的稀盐酸在锥形瓶中反应(样品中杂质不与稀盐酸反应),实验装置如右图所示.每2分钟读取一次电子天平的示数,据此计算生成的二氧化碳的质量,前18分钟数据记录见下表:
(1)实验过程中,通过观察装置中的哪一现象可判断反应结束?不再产生气泡
(2)结合表格分析,块状大理石与稀盐酸反应最多能产生2.40克二氧化碳.
(3)当反应进行到l8分钟时,块状大理石中有多少克碳酸钙与稀盐酸发生了反应?(写出计
算过程) (CaCO3+2HCl=CaCl2+H2O+CO2↑)
 为研究影响化学反应快慢的因素,小明选取成分相同的大理石碎屑、块状大理石两种样品各6克,分别与足量的、溶质质量分数相同的稀盐酸在锥形瓶中反应(样品中杂质不与稀盐酸反应),实验装置如右图所示.每2分钟读取一次电子天平的示数,据此计算生成的二氧化碳的质量,前18分钟数据记录见下表:
为研究影响化学反应快慢的因素,小明选取成分相同的大理石碎屑、块状大理石两种样品各6克,分别与足量的、溶质质量分数相同的稀盐酸在锥形瓶中反应(样品中杂质不与稀盐酸反应),实验装置如右图所示.每2分钟读取一次电子天平的示数,据此计算生成的二氧化碳的质量,前18分钟数据记录见下表:| 时间/分 | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 |
| 大理石碎屑生成的C02质量/克 | 0 | 1.45 | 1.75 | 1.98 | 2.18 | 2.30 | 2.36 | 2.40 | 2.40 | 2.40 |
| 块状大理石生成的C02质量/克 | O | 0.45 | 0.80 | 1.10 | 1.36 | 1.60 | 1.81 | 1.98 | 2.11 | 2.20 |
(2)结合表格分析,块状大理石与稀盐酸反应最多能产生2.40克二氧化碳.
(3)当反应进行到l8分钟时,块状大理石中有多少克碳酸钙与稀盐酸发生了反应?(写出计
算过程) (CaCO3+2HCl=CaCl2+H2O+CO2↑)
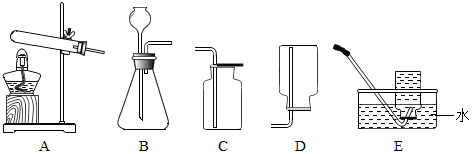
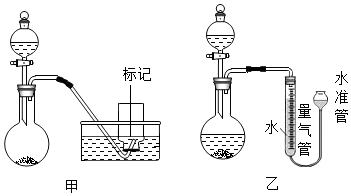
 如图为精制粗盐的示意图,回答:
如图为精制粗盐的示意图,回答: