题目内容
12.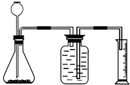 利用如图装置能制取氢气并测定所收集气体的体积.毛毛同学在锥形瓶中装入13g锌粒,往长颈漏斗中加入100g稀硫酸,两者恰好完全反应(反应原理Zn+H2SO4=ZnSO4+H2↑).
利用如图装置能制取氢气并测定所收集气体的体积.毛毛同学在锥形瓶中装入13g锌粒,往长颈漏斗中加入100g稀硫酸,两者恰好完全反应(反应原理Zn+H2SO4=ZnSO4+H2↑).(1)若要收集300mL氢气,应选用500mL(填“10”或“100”或“500”)量筒
(2)求产生氢气的质量
(3)求稀硫酸的溶质质量分数
(4)求反应后溶液的溶质质量分数.
分析 (1)根据量筒的选用采用就近原则进行分析;
(2)根据锌与硫酸反应的化学方程式,依据锌粒的质量计算生成氢气的质量和参加反应的硫酸的质量,生成的硫酸锌的质量;
(3)根据计算出的硫酸计算稀硫酸的溶质质量分数;
(4)根据计算出的硫酸锌计算反应后溶液的溶质质量分数.
解答 解:(1)量筒的选用采用就近原则,所以若要收集300mL氢气,应选用500mL的量筒;
(2)设生成氢气的质量为x,参加反应的硫酸质量为y,生成硫酸锌的质量为z,
Zn+H2SO4═ZnSO4+H2↑
65 98 161 2
13g y z x
$\frac{65}{13g}$=$\frac{98}{y}$=$\frac{161}{z}$=$\frac{2}{x}$
x=0.4g
y=19.6g
z=32.2g
所以稀硫酸的溶质质量分数为:$\frac{19.6g}{100g}$×100%=19.6%;
所以反应后溶液的溶质质量分数为:$\frac{32.2g}{100g+13g-0.4g}$×100%=28.6%.
故答案为:(1)500;
(2)氢气质量0.4g;
(3)硫酸溶液质量分数:19.6%;
(4)反应后溶液质量分数:28.6%.
点评 在使用量筒量取液体体积时,选用量筒应遵循一次性原则即选用量筒的量程稍大于所要量取液体的体积而一次性测量,以保证测量的精确度.

练习册系列答案
相关题目
3.下列符号中,表示一种元素,又表示这种元素的一个原子,还表示这种元素所形成的单质的化学式( )
| A. | H | B. | Fe | C. | N2 | D. | O |
7.空气是一种宝贵的自然资源.下列有关说法中不正确的是( )
| A. | 空气中由氮气、氧气、稀有气体、二氧化碳等物质组成的混合物 | |
| B. | 法国化学家拉瓦锡研究了空气的成分,并得出氧气约占空气总体积$\frac{4}{5}$的结论 | |
| C. | 氮气是制造硝酸和氮肥的重要原料 | |
| D. | 稀有气体都没有颜色、没有气味,在通电时能发出不同颜色的光 |
17.某密闭容器中有X、Y、Z、W 四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下
下列说法正确的是( )
| 物质 | X | Y | Z | W |
| 反应前质量 | 4 | 1 | 10 | 2 |
| 反应后质量 | 待测 | 5 | 4 | 8 |
| A. | 参加反应的X和Z的质量之比是2:3 | B. | Z与W的相对分子质量比一定是1:1 | ||
| C. | 该反应的反应物只有Z | D. | 反应后X的质量为8g |
4.现将8gA和足量B混合加热,A和B发生化学反应,8gA完全反应后生成6gC和4gD,则参加反应的A与B质量比是( )
| A. | 1:1 | B. | 2:1 | C. | 4:l | D. | 5:1 |


