题目内容
1.水体污染的主要来源有哪些?提出相应的防治措施.分析 根据水污染的来源回答.随着工农业生产的快速发展,环境污染相当严重.
解答 解:水污染的来源主要有工业污染、农业污染和生活污染;
防治水污染的措施有:工业废水、农业废水和生活污水处理后再排放,农业上合理使用化肥和农药等.
故答案为:工业污染、农业污染和生活污染;工业废水、农业废水和生活污水处理后再排放,农业上合理使用化肥和农药等.
点评 不但水污染很严重,空气、土壤污染也很严重,因此要保护环境,防止环境污染.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
6.为了测定某赤铁矿中氧化铁的质量分数,现取赤铁矿样品,与质量分数为19.6%的稀硫酸在烧杯(烧杯质量为50g)中恰好完全反应(假设赤铁矿样品中杂质不与稀硫酸反应也不溶于水).有关实验数据如下表:
(1)配制上述质量分数为19.6%的稀硫酸,需要质量分数为98%的浓硫酸的质量是30g;
(2)发生反应的化学方程式为Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;
(3)利用已知条件求解氧化铁质量(X)的比例式为$\frac{160}{x}$=$\frac{294}{150g×19.6%}$;
(4)向反应后所得溶液中加入34g水,则最终溶液中溶质的质量分数是20%;
(5)利用150t该赤铁矿可制得含杂质的生铁的质量是114t.
| 反应前 | 反应后 | ||
| 实验 数据 | 烧杯和稀硫酸的质量 | 赤铁矿样品的质量 | 烧杯和混合物的质量 |
| 200g | 20g | 220g | |
(2)发生反应的化学方程式为Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;
(3)利用已知条件求解氧化铁质量(X)的比例式为$\frac{160}{x}$=$\frac{294}{150g×19.6%}$;
(4)向反应后所得溶液中加入34g水,则最终溶液中溶质的质量分数是20%;
(5)利用150t该赤铁矿可制得含杂质的生铁的质量是114t.
10.生活中化学无处不在,下列说法错误的是( )
| A. | 活性炭可以除去冰箱中的异味 | |
| B. | 胃酸过多可适量服用氢氧化钙溶液 | |
| C. | 为增强肥效,将钾肥草木灰和氮肥硝铵混合使用 | |
| D. | 血红蛋白中含有铁元素,缺铁会引起人体贫血 |
11.空气是人类最宝贵的自然资源.空气中氮气的含量最多,氮气在高温、高能量条件下可与某些物质发生反应.图1是以空气和其他必要的原料合成氮肥(NH4HCO3)的流程.请按要求回答下列问题:
(1)步骤①中可利用氮气和氧气的沸点不同分离出氮气和氧气.
(2)写出步骤②中发生反应的化学式表达式3H2+N2$\frac{\underline{\;一定条件\;}}{\;}$2NH3.
(3)图2是化肥碳酸氢铵包装袋上的部分说明:碳酸氢铵具有的性质是AC(填字母).
A.易溶于水 B.有挥发性 C.受热易分解
(4)这种化肥含氮量是否达到16%,化肥中碳酸氢铵的含量是多少?带着这些问题,兴趣小组的同学取了一些化肥样品,进入实验室.
【查找资料】①碱石灰能够吸收水和CO2,但是不吸收NH3.
②浓硫酸能吸收NH3但是不吸收CO2.
③氨气溶于水形成氨水
【性质探究】该同学设计了如图3的实验装置:

①用A装置给碳酸氢铵加热,装药品前,必须进行的一步操作是检验装置气密性.
②取适量碳酸氢铵加入试管,连接A、C、E装置,加热,E中的现象是无色酚酞试液变红.
③连接A、B装置,继续加热,观察到试管口的现象是有水滴,B中的现象是变浑浊.
④碳酸氢铵在受热时发生反应的化学式表达式是NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑.
【含量分析】将装置A、C、D依次连接,加入20g化肥样品,加热至A中固体完全消失.
她称量装置D的质量如表:
⑤由此分析得知:反应中产生氨气的质量为3.4g.
⑥通过反应的表达式可以知道:氨气中氮元素全部来自于碳酸氢铵(假设杂质中不含氮元素),请计算此化肥含氮元素质量分数为14%.
⑦请计算此化肥中碳酸氢铵的纯度79%.
⑧20千克的硝酸铵(NH4NO3)和这袋化肥的含氮元素质量相等.

(1)步骤①中可利用氮气和氧气的沸点不同分离出氮气和氧气.
(2)写出步骤②中发生反应的化学式表达式3H2+N2$\frac{\underline{\;一定条件\;}}{\;}$2NH3.
(3)图2是化肥碳酸氢铵包装袋上的部分说明:碳酸氢铵具有的性质是AC(填字母).
A.易溶于水 B.有挥发性 C.受热易分解
(4)这种化肥含氮量是否达到16%,化肥中碳酸氢铵的含量是多少?带着这些问题,兴趣小组的同学取了一些化肥样品,进入实验室.
【查找资料】①碱石灰能够吸收水和CO2,但是不吸收NH3.
②浓硫酸能吸收NH3但是不吸收CO2.
③氨气溶于水形成氨水
【性质探究】该同学设计了如图3的实验装置:

①用A装置给碳酸氢铵加热,装药品前,必须进行的一步操作是检验装置气密性.
②取适量碳酸氢铵加入试管,连接A、C、E装置,加热,E中的现象是无色酚酞试液变红.
③连接A、B装置,继续加热,观察到试管口的现象是有水滴,B中的现象是变浑浊.
④碳酸氢铵在受热时发生反应的化学式表达式是NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑.
【含量分析】将装置A、C、D依次连接,加入20g化肥样品,加热至A中固体完全消失.
她称量装置D的质量如表:
| 实验前D装置的质量 | 149g |
| 实验后D装置的质量 | 152.4g |
⑥通过反应的表达式可以知道:氨气中氮元素全部来自于碳酸氢铵(假设杂质中不含氮元素),请计算此化肥含氮元素质量分数为14%.
⑦请计算此化肥中碳酸氢铵的纯度79%.
⑧20千克的硝酸铵(NH4NO3)和这袋化肥的含氮元素质量相等.

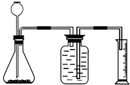 利用如图装置能制取氢气并测定所收集气体的体积.毛毛同学在锥形瓶中装入13g锌粒,往长颈漏斗中加入100g稀硫酸,两者恰好完全反应(反应原理Zn+H2SO4=ZnSO4+H2↑).
利用如图装置能制取氢气并测定所收集气体的体积.毛毛同学在锥形瓶中装入13g锌粒,往长颈漏斗中加入100g稀硫酸,两者恰好完全反应(反应原理Zn+H2SO4=ZnSO4+H2↑).