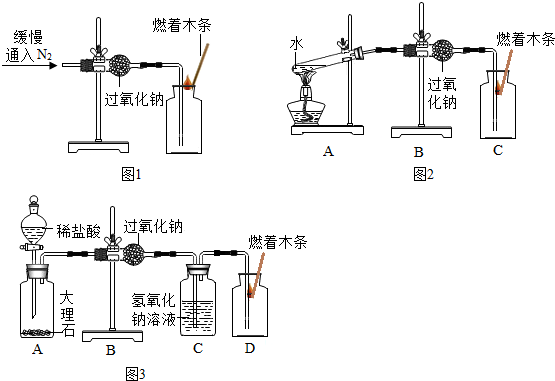
题目内容
某碳酸钾固体样品,可能含有硫酸钾、碳酸钠、硫酸铜、氯化钾、氯化钙中的一种或几种杂质.张乐为了确定杂质的成分,进行了以下实验,根据实验现象及下表中的信息回答下列问题.
①取少量样品溶于水得到蓝色溶液,然后滴加过量的氯化钡溶液,出现白色沉淀A,过滤.
②沉淀A中加入过量的稀硝酸,沉淀部分消失并放出气体.
③往步骤①所得的滤液中加入适量硝酸银溶液和稀硝酸,生成白色沉淀B.
(1)白色沉淀A是 和 混合物,白色沉淀B是 .
(2)杂质中一定含有 ,一定没有 .
①取少量样品溶于水得到蓝色溶液,然后滴加过量的氯化钡溶液,出现白色沉淀A,过滤.
②沉淀A中加入过量的稀硝酸,沉淀部分消失并放出气体.
③往步骤①所得的滤液中加入适量硝酸银溶液和稀硝酸,生成白色沉淀B.
(1)白色沉淀A是
(2)杂质中一定含有
NO
| Cl- | SO
| CO
| |||||||
| K+ | 溶 | 溶 | 溶 | 溶 | ||||||
| Ca2+ | 溶 | 溶 | 溶 | 不 | ||||||
| Ba2+ | 溶 | 溶 | 不 | 不 | ||||||
| Ag+ | 溶 | 不 | 溶 | 不 |
考点:物质的鉴别、推断,盐的化学性质
专题:混合物组成的推断题
分析:根据硫酸铜在溶液中显蓝色,硫酸根离子、碳酸根离子与钡离子会生成白色的硫酸钡沉淀、碳酸钡沉淀,碳酸钡沉淀会溶于硝酸,硫酸钡沉淀不溶于硝酸,氯离子和银离子会生成氯化银沉淀,氯化银沉淀不溶于硝酸等知识进行分析.
解答:解:取少量样品溶于水得到蓝色溶液,所以杂质中一定含硫酸铜,不含能够和碳酸钾反应产生沉淀的氯化钙,然后滴加过量的氯化钡溶液,出现白色沉淀A,过滤,沉淀A中加入过量的稀硝酸,沉淀部分消失并放出气体,该沉淀一定有碳酸钾反应产生的碳酸钡沉淀、硫酸铜反应产生的硫酸钡沉淀;往步骤①所得的滤液中加入适量硝酸银溶液和稀硝酸,生成白色沉淀B,说明沉淀是氯化银,由于步骤①中加入的过量氯化钡,所以步骤①所得的滤液中含有氯离子,因此杂质中可能含有氯化钾.
(1)通过推导可知,不是沉淀A是碳酸钡和硫酸钡,白色沉淀B是氯化银;
(2)通过推导可知,杂质中一定含有硫酸铜,一定没有氯化钙;
故答案为:(1)碳酸钡、硫酸钡;氯化银;(2)硫酸铜;氯化钙.
(1)通过推导可知,不是沉淀A是碳酸钡和硫酸钡,白色沉淀B是氯化银;
(2)通过推导可知,杂质中一定含有硫酸铜,一定没有氯化钙;
故答案为:(1)碳酸钡、硫酸钡;氯化银;(2)硫酸铜;氯化钙.
点评:在解此类题时,首先分析所给物质的性质和两两之间的反应,然后结合题中的现象确定各物质的存在性,最后进行验证即可.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
宣传科学知识,反对伪科学是我们应尽的责任.下列说法具有科学道理的是( )
| A、干冰用于人工降雨 |
| B、用催化剂将水变成燃油 |
| C、人们可用肉眼看到硅原子 |
| D、中药是纯天然的,绝不含任何化学物质 |
酸碱中和反应,在日常生活生产中应用广泛.张萌列举的实际应用中,属于利用中和反应原理的是( )
①用碳酸钙与盐酸反应制取二氧化碳
②用小苏打治疗胃酸过多
③用熟石灰改良酸性土壤
④用稀氨水涂抹在蚊子叮咬处(分泌出蚁酸)止痒.
①用碳酸钙与盐酸反应制取二氧化碳
②用小苏打治疗胃酸过多
③用熟石灰改良酸性土壤
④用稀氨水涂抹在蚊子叮咬处(分泌出蚁酸)止痒.
| A、①② | B、②③④ |
| C、③④ | D、①③④ |
燃烧是人类最早利用的化学反应之一,下列叙述中正确的是( )
| A、物质在氧气中燃烧的反应一定是化合反应 |
| B、物质与氧气发生的反应都是燃烧 |
| C、木炭需要加热到一定温度时才燃烧,所以木炭燃烧是吸热反应 |
| D、化学反应在生成新物质的同时,还伴随着能量的变化 |
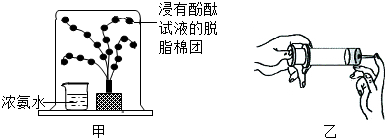 根据图中的相关信息回答下列问题.
根据图中的相关信息回答下列问题.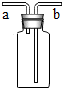 如图有多种功能,如收集气体、洗涤气体、贮存气体等.回答下列问题
如图有多种功能,如收集气体、洗涤气体、贮存气体等.回答下列问题