题目内容
15.某实验需要100g16%的硫酸铜溶液.(1)实验室用硫酸铜晶体(化学式为CuSO4.5H2O)配制该硫酸铜溶液,需称取硫酸铜晶体25gg.
(2)该溶液若用40%的硫酸铜溶液来配制,则需加水60g.
分析 (1)利用溶质质量=溶液质量×溶质的质量分数,硫酸铜晶体是CuSO4.5H2O,进行分析解答.
(2)根据溶液稀释前后溶质的质量不变,结合题意进行分析解答.
解答 解:(1)利用溶质质量=溶液质量×溶质的质量分数,配制100g16%的硫酸铜溶液,需要硫酸铜的质量为100g×16%=16g;则需要硫酸铜晶体的质量为16g÷($\frac{64+32+16×4}{64+32+16×4+(1×2+16)×5}$×100%)=25g.
(2)设要加水的质量为x,根据溶液稀释前后溶质的质量不变,
则100g×16%=(100g-x)×40% x=60g.
故答案为:(1)25g;(2)60.
点评 本题难度不大,掌握溶质质量=溶液质量×溶质的质量分数、溶液稀释前后溶质的质量不变是正确解答本题的关键所在.

练习册系列答案
相关题目
5.下列关于催化剂的说法中,正确的是( )
| A. | 加入催化剂能使化学反应的速率加快 | |
| B. | 不使用催化剂物质就不能发生化学反应 | |
| C. | 使用催化剂可增加生成物的量 | |
| D. | 使用催化剂能改变化学反应的速率 |
6.为了测定某赤铁矿中氧化铁的质量分数,现取赤铁矿样品,与质量分数为19.6%的稀硫酸在烧杯(烧杯质量为50g)中恰好完全反应(假设赤铁矿样品中杂质不与稀硫酸反应也不溶于水).有关实验数据如下表:
(1)配制上述质量分数为19.6%的稀硫酸,需要质量分数为98%的浓硫酸的质量是30g;
(2)发生反应的化学方程式为Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;
(3)利用已知条件求解氧化铁质量(X)的比例式为$\frac{160}{x}$=$\frac{294}{150g×19.6%}$;
(4)向反应后所得溶液中加入34g水,则最终溶液中溶质的质量分数是20%;
(5)利用150t该赤铁矿可制得含杂质的生铁的质量是114t.
| 反应前 | 反应后 | ||
| 实验 数据 | 烧杯和稀硫酸的质量 | 赤铁矿样品的质量 | 烧杯和混合物的质量 |
| 200g | 20g | 220g | |
(2)发生反应的化学方程式为Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;
(3)利用已知条件求解氧化铁质量(X)的比例式为$\frac{160}{x}$=$\frac{294}{150g×19.6%}$;
(4)向反应后所得溶液中加入34g水,则最终溶液中溶质的质量分数是20%;
(5)利用150t该赤铁矿可制得含杂质的生铁的质量是114t.
10.生活中化学无处不在,下列说法错误的是( )
| A. | 活性炭可以除去冰箱中的异味 | |
| B. | 胃酸过多可适量服用氢氧化钙溶液 | |
| C. | 为增强肥效,将钾肥草木灰和氮肥硝铵混合使用 | |
| D. | 血红蛋白中含有铁元素,缺铁会引起人体贫血 |
7.某同学将白磷在密闭容器中引燃,反应完后,你认为容器内的总质量在反应前后如何变化( )
| A. | 减少 | B. | 增加 | C. | 相等 | D. | 无法确定 |
5.亚硒酸钠能抗衰老,由硒、氧、钠三种元素组成,其中硒(Se)为+4价,则亚硒酸钠的化学式为( )
| A. | Na2SeO3 | B. | Na2SeO4 | C. | NaSeO3 | D. | Na2SeO2 |
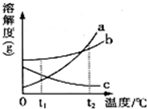 图是a、b、c三种固体物质的溶解度曲线,请回答
图是a、b、c三种固体物质的溶解度曲线,请回答


