题目内容
有一包白色固体可能含碳酸钠、硫酸钠、氯化钾、硝酸钡、氢氧化钠中的一种或几种.某化学兴趣小组为探究其成分做了以下实验:
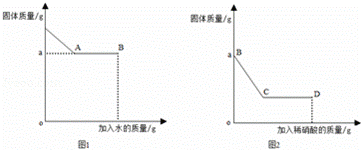
Ⅰ.取少量固体于烧杯中,逐渐加水并不断搅拌,烧杯内固体的质量随加入水的质量的变化如图1所示;
Ⅱ.取少量B点时的清液于试管中,滴加酚酞溶液,酚酞溶液不变色;
Ⅲ.继续向烧杯中滴加稀硝酸并不断搅拌,烧杯内固体的质量随加入稀硝酸的质量的变化如图2所示.
请回答下列问题:
(1)BC段可观察到的现象是 ,从C到D液体的pH (填“增大”、“减小”或“不变”);
(2)原白色固体中一定含有 ,可能含有 ;
(3)D点时,溶液中一定含有的溶质是 ;
(4)为进一步探究该白色固体的成分,该组同学取少量原固体样品于试管中,加足量水溶解,加 ,过滤;再向滤液中加 ,观察现象.
考点:
物质的鉴别、推断;碱的化学性质;盐的化学性质.
专题:
混合物组成的推断题.
分析:
碳酸钠、硫酸钠、氯化钾、硝酸钡、氢氧化钠都是可溶于水的物质,由图1可知,加入水,有不溶物,说明了上述物质间发生反应生成了沉淀,由于碳酸能、硫酸钠都能与硝酸钡反应生成沉淀,由此可知,一定存在硝酸钡;由图2可知沉淀加入稀硝酸沉淀部分溶解,沉淀应为碳酸钡和硫酸钡的混合物,说明了原混合物中一定有碳酸钠和硫酸钠.由取少量B点时的清液于试管中,滴加酚酞溶液,酚酞溶液不变色,说明了不含有氢氧化钠,据此分析回答有关的问题.
解答:
解:由图1可知,加入水,有不溶物,说明了上述物质间发生反应生成了沉淀,由于碳酸能、硫酸钠都能与硝酸钡反应生成沉淀,由此可知,一定存在硝酸钡;由图2可知沉淀加入稀硝酸后,沉淀部分溶解,沉淀应为碳酸钡和硫酸钡的混合物,说明了原混合物中一定有碳酸钠和硫酸钠;由取少量B点时的清液于试管中,滴加酚酞溶液,酚酞溶液不变色,说明了不含有氢氧化钠.
(1)由上述分析可知,BC段可观察到的现象是固体部分溶解,有气泡冒出,从C到D液体的酸性增强,液体的pH减小;
(2)由上述分析可知,原白色固体中一定含有碳酸钠、硫酸钠、硝酸钡,可能含有氯化钾;
(3)D点时,溶液中一定含有的溶质是硝酸钠、硝酸钡、硝酸;
(4)由于氯化钾的存在不能确定,为进一步探究该白色固体的成分,该组同学取少量原固体样品于试管中,加足量水溶解,加稀硝酸,过滤;再向滤液中加硝酸银,观察现象,若有白色沉淀生成则证明含有氯化钾,否则则没有.
故答为:(1)固体部分溶解,有气泡冒出,减小;
(2)碳酸钠、硫酸钠、硝酸钡,氯化钾;
(3)硝酸钠、硝酸钡、硝酸;
(4)稀硝酸,硝酸银.
点评:
本题主要考查了物质的鉴别和推断,难度稍大,了解碳酸根离子、硫酸根离子、氯离子的检验方法是解答本题的关键.

化学就在我们身边.下表是生活中常见的两种清洁剂.且NaClO+2HCl=NaCl+X↑+H2O.则下列说法正确的是( )
| 清洁剂名称 | 洁厕灵 | 84消毒液 |
| 有效成分 | HCl | NaClO |
|
| A. | “洁厕灵”可用于金属表面除锈 |
|
| B. | “洁厕灵”可用于清洁大理石地面 |
|
| C. | “84消毒液”中NaClO属于盐,其中Cl元素的化合价呈﹣1价 |
|
| D. | “洁厕灵”与“84消毒液”混合后发生置换反应 |
下列说法错误的是( )
|
| A. | NO2和Fe2O3都是氧化物 |
|
| B. | 生铁和钢都是铁合金 |
|
| C. | 空气和液氧都是混合物 |
|
| D. | 金刚石和石墨都是由碳元素组成的单质 |
下列有关实验操作及分析均合理的是( )
|
| A. | 排水法收集O2:导气管口刚有气泡冒出立即收集,收集到的O2更纯净 |
|
| B. | 去除粗盐中难溶性杂质:将粗盐全部加入水中立即过滤,导致产率偏低 |
|
| C. | 测定空气里O2含量:点燃红磷慢慢伸入集气瓶并塞紧瓶塞,导致测定结果偏低 |
|
| D. | 探究CO2性质:将CO2快速倒入盛有燃着蜡烛的烧杯中,便于观察低处蜡烛先熄灭 |

 ,请回答下列问题:①X阳离子的离子结构示意图为 ,W离子的离子符号为 ;
,请回答下列问题:①X阳离子的离子结构示意图为 ,W离子的离子符号为 ;