题目内容
5. 小廷同学在实验室将5%的NaOH溶液逐滴加入到14g稀盐酸中,边加边搅拌,随着NaOH溶液的不断加入,溶液pH的变化如图所示,请回答
小廷同学在实验室将5%的NaOH溶液逐滴加入到14g稀盐酸中,边加边搅拌,随着NaOH溶液的不断加入,溶液pH的变化如图所示,请回答(1)a点溶液中含有的阳离子有Na+、H+.
(2)当pH=7时,消耗NaOH的质量为0.8g.
(3)求恰好完全反应时溶液中溶质的质量分数(精确到0.1%)
分析 (1)稀盐酸和氢氧化钠反应生成氯化钠和水,在a点时,溶液的pH小于7,说明加入的氢氧化钠的量不足,稀盐酸由剩余,溶液中大量存在的阳离子是钠离子和氢离子;
(2)根据图中信息可以判断当恰好完全反应时,消耗NaOH溶液的质量,再根据溶质质量分数的计算公式计算 NaOH的质量;
(3)根据氢氧化钠溶液质量、溶质质量分数可以计算氯化钠的质量,进一步可以计算恰好完全反应时溶液中溶质的质量分数.
解答 解:(1)a点时氢氧化钠与氯化氢恰好反应生成氯化钠,则该溶液中大量存在的离子为:Na+、H+,
故答案为:Na+、H+;
(2)根据图示可知,两溶液恰好完全反应时消耗NaOH溶液的质量为16g,氢氧化钠的质量为16g×5%=0.8g
故答案为:0.8;
(3)设恰好完全反应时溶液中溶质的质量为x,
NaOH+HCl═NaCl+H2O,
40 58.5
16g×5% x
则:$\frac{40}{58.5}=\frac{16g×5%}{x}$ 解得:x=1.17g,
恰好完全反应时溶液中溶质的质量分数:$\frac{1.17g}{16g+14g}$×100%=3.9%,
答:恰好完全反应时溶液中溶质的质量分数为39%.
点评 本题考查了酸碱混合的定性判断及计算,题目难度不大,明确中和反应的实质为解答关键,注意掌握溶液酸碱性与溶液pH的关系,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
16.下列关于结晶和晶体的说法,错误的是( )
| A. | 饱和溶液降温析出晶体后的溶液仍是饱和溶液(指降温后的溶液) | |
| B. | 降低饱和溶液的温度,不一定有晶体析出 | |
| C. | 从溶液中析出的晶体不一定都含有结晶水 | |
| D. | 从饱和硫酸铜溶液结晶析出的胆矾是混合物 |
13.今年5月,我国科学家首次实现了在催化剂的作用下CO2直接与H2反应合成汽油,该研究成果已经申报发明专利.下列说法错误的是( )
| A. | 这个发明的大规模生产有利于减缓温室效应 | |
| B. | 这个反应是利用无机物生成有机化合物 | |
| C. | 石油和用CO2制造的汽油都是不可再生能源 | |
| D. | 汽油的组成中一定含有碳氢元素 |
20.只用一种试剂(括号内的物质),不能将组内的物质鉴别出来的是( )
| A. | Ca(OH)2、NaCl、Na2SO4、H2SO4四种溶液(碳酸钠溶液) | |
| B. | CuO、Fe、C、Al四种固体粉末(稀硫酸) | |
| C. | NH4NO3、NaOH、CaO、Na2CO3四种白色固体(水) | |
| D. | CO2、O2、H2、空气四种无色气体(燃着的木条) |
10.我们每时每刻都离不开空气.下列有关空气及其成分的说法正确的是( )
| A. | 空气中体积分数最大的气体是氧气 | |
| B. | 鱼能在水中生存,说明氧气易溶于水 | |
| C. | 空气中可吸入颗粒物的多少不会影响人体健康 | |
| D. | 稀有气体在通电时能发出不同颜色的光,可用作电光源 |
1.如图所示的微观变化与下列反应及反应类型对应正确的是( )
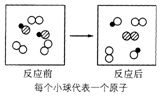

| A. | 2CO+O2 $\frac{\underline{\;点燃\;}}{\;}$2CO2 化合反应 | |
| B. | 2HI+Cl2═2HCl+I2 置换反应 | |
| C. | 2H2O $\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑ 分解反应 | |
| D. | 2HCl+CuO═CuCl2+H2O 复分解反应 |
18.某市有一家工厂处理含铜垃圾的生产流程如下,下列有关说法正确的是( )


| A. | 步骤①用灼烧法是因为铜能在空气中燃烧 | |
| B. | 步骤②反应后所得的蓝色溶液不可能呈酸性 | |
| C. | ③和⑤两步骤中均有过滤操作 | |
| D. | 步骤④发生的反应类型是复分解反应 |
 A、B、C、D、E、F为初中化学中常见的物质,它们之间有如图所示的反应关系(“→”表示能转化,“-”表示能发生反应,部分产物已略去),其中C是大理石的主要成分,E是最常用的溶剂,F由三种元素组成,其相对分子质量为40.回答下列问题:
A、B、C、D、E、F为初中化学中常见的物质,它们之间有如图所示的反应关系(“→”表示能转化,“-”表示能发生反应,部分产物已略去),其中C是大理石的主要成分,E是最常用的溶剂,F由三种元素组成,其相对分子质量为40.回答下列问题: 同学们都知道“木糖醇口香糖”吧?经研究表明木糖醇的甜度高,溶解性好,防龋齿,是一种理想的蔗糖替代品,适合糖尿病患者食用.木糖醇和蔗糖的溶解度曲线如图,据图回答
同学们都知道“木糖醇口香糖”吧?经研究表明木糖醇的甜度高,溶解性好,防龋齿,是一种理想的蔗糖替代品,适合糖尿病患者食用.木糖醇和蔗糖的溶解度曲线如图,据图回答