题目内容
14.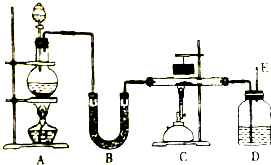 化学实验室常用甲酸(HCOOH)和浓硫酸混合加热制备一氧化碳,其化学方程式为:HCOOH$\frac{\underline{\;浓H_{2}SO_{4}\;}}{△}$CO↑+H2O,如图是制备干燥一氧化碳还原氧化铁并检验反应产物的实验装置.
化学实验室常用甲酸(HCOOH)和浓硫酸混合加热制备一氧化碳,其化学方程式为:HCOOH$\frac{\underline{\;浓H_{2}SO_{4}\;}}{△}$CO↑+H2O,如图是制备干燥一氧化碳还原氧化铁并检验反应产物的实验装置.(1)为顺利、安全地完成实验,实验开始时既要检查装置的气密性,还应检验一氧化碳纯度,以防爆炸.
(2)装置B中盛放碱石灰,作用是除去水蒸气.
(3)装置D中盛放澄清石灰水,检验产物二氧化碳.
(4)写出装置D中反应的化学方程式Ca(OH)2+CO2=CaCO3↓+H2O.
(5)实验开始时,应先点燃A处酒精灯(填“A处酒精灯”或“C处酒精喷灯”,下同),实验结束时应先停止C处酒精喷灯的加热,本实验的不足之处是E处应该加酒精灯点燃.
(6)在反应后磁铁悬在玻璃管上方,其作用是将铁从混合物中分离出来.
分析 (1)根据一氧化碳和空气的混合气点燃可能发生爆炸进行分析;
(2)根据碱石灰具有吸水性进行分析;
(3)根据氢氧化钙会与二氧化碳反应生成碳酸钙沉淀进行分析;
(4)根据氢氧化钙会与二氧化碳反应生成碳酸钙沉淀和水进行分析;
(5)根据实验开始时,应先点燃A处酒精灯制取一氧化碳,实验结束时应先停止C处酒精喷灯,防止高温的铁重新氧化,一氧化碳需要尾气处理进行分析;
(6)根据磁铁能够吸引铁,可以把铁和其它物质组成的混合物分离,从而得到铁进行分析.
解答 解:(1)一氧化碳和空气的混合气点燃可能发生爆炸,所以实验开始时既要检查装置的气密性,还应检验一氧化碳纯度,以防爆炸;
(2)碱石灰具有吸水性,所以装置B中盛放碱石灰,作用是除去水蒸气;
(3)氢氧化钙会与二氧化碳反应生成碳酸钙沉淀,所以装置D中盛放澄清石灰水,检验产物二氧化碳;
(4)氢氧化钙会与二氧化碳反应生成碳酸钙沉淀和水,化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;
(5)实验开始时,应先点燃A处酒精灯制取一氧化碳,实验结束时应先停止C处酒精喷灯,防止高温的铁重新氧化,一氧化碳需要尾气处理;
(6)磁铁能够吸引铁,可以把铁和其它物质组成的混合物分离,从而得到铁.
故答案为:(1)一氧化碳纯度;
(2)碱石灰,除去水蒸气;
(3)澄清石灰水,产物二氧化碳;
(4)Ca(OH)2+CO2=CaCO3↓+H2O;
(5)A处酒精灯,C处酒精喷灯,;
(6)将铁从混合物中分离出来.
点评 本题考查了基本实验的设计,难度不大,注意该实验起始时一定检验CO的纯度,否则可能有安全事故发生.

练习册系列答案
相关题目
6.下列用途,主要是利用了该物质化学性质的是( )
| A. | 用氮气填充灯泡 | B. | 用稀有气体制作霓虹灯 | ||
| C. | 用氦气填充气球 | D. | 用金属铜做电线 |
2. 要使如图装置中的小气球鼓起来,则使用的固体和液体可以是( )
要使如图装置中的小气球鼓起来,则使用的固体和液体可以是( )
①石灰石和稀盐酸
②镁和稀硫酸
③固体氢氧化钠和水
④过氧化氢溶液和二氧化锰.
 要使如图装置中的小气球鼓起来,则使用的固体和液体可以是( )
要使如图装置中的小气球鼓起来,则使用的固体和液体可以是( )①石灰石和稀盐酸
②镁和稀硫酸
③固体氢氧化钠和水
④过氧化氢溶液和二氧化锰.
| A. | ①②③④ | B. | ①②③ | C. | ①②④ | D. | ②③④ |
 图中:“
图中:“ ”表示氧原子,“
”表示氧原子,“ ”表示氢原子,用化学用语表示框内物质.
”表示氢原子,用化学用语表示框内物质.